
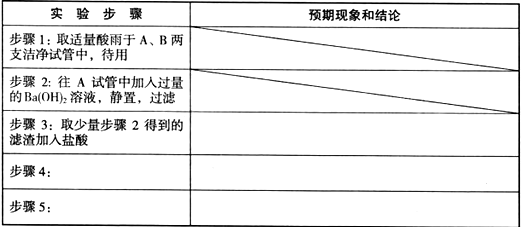
| 实验步骤 | 预期现象和结论 |
| 步骤3: | 若滤渣不完全溶解,则酸雨中含硫酸 |
| 步骤4:取适量步骤2得到的滤液,先加入过量的硝酸,然后加入AgNO3溶液 | 若产生白色沉淀,则酸雨中含盐酸 |
| 步骤5:往B试管中加入少量品红溶液,振荡 | 若品红溶液褪色,则酸雨中含亚硫酸或SO2 |


科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该溶液中一定含有 CO32- |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
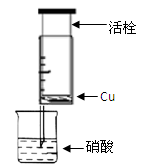
| 组 | m(Cu)/g | 硝酸(过量) | 溶液颜色 |
| A | 1 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| B | 0.5 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| C | 2 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.称取一定质量的NaCl,用纸槽小心地加入到容量瓶中,然后用量筒量取一定量的水加入容量瓶中,配制准确浓度的NaCl溶液 |
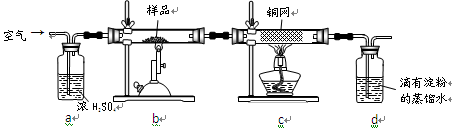
| B.实验室用如右图所示装置可制取乙烯并验证 乙烯的某些化学性质 |
| C.用足量的稀盐酸与MnO2在加热条件下,可制得氯气 |
| D.用澄清的石灰水溶液来区别碳酸钠、碳酸氢钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
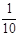 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.10mL,末读数如右图所示。
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.10mL,末读数如右图所示。

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 实现现象 | 反应的离子方程式 |
| 往滤渣中加入过量NaOH溶液。 | | ① |
| 过滤,往所得滤液中通入过量二氧化碳, | ② | ③ |
| 继续加入过量稀盐酸 | ④ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | A | B | C | D |
| 实验 目的 | 除去碳酸钠中少量的碳酸氢钠 | 清洗铁制品 表面的铁锈 | 检验苯中 含有少量甲苯 | 鉴别二氧化氮 和溴蒸汽 |
| 方案1 | 溶解后加入盐酸 | 加适量稀盐酸 | 加入Br2/CCl4 | 加水 |
| 方案2 | 加热 | 用水洗涤 | 加入酸性KMnO4 | 加压 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com