
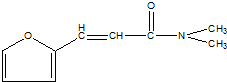
 是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )
是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )| A. | 12种 | B. | 15种 | C. | 18种 | D. | 21种 |
分析 有机物 的不饱和度为5,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基,所以剩余2个碳原子,取代基可以为:-CH2CH2COOH和-NH2,-CH(COOH)CH3和-NH2,-CH2CH2NH2和-COOH,-CH(NH2)CH3和-COOH,--CH2(NH2)COOH和-CH3,-CH2COOH和-CH2NH2,两个取代基又分为邻、间、对三种情况.
的不饱和度为5,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基,所以剩余2个碳原子,取代基可以为:-CH2CH2COOH和-NH2,-CH(COOH)CH3和-NH2,-CH2CH2NH2和-COOH,-CH(NH2)CH3和-COOH,--CH2(NH2)COOH和-CH3,-CH2COOH和-CH2NH2,两个取代基又分为邻、间、对三种情况.
解答 解:有机物 的不饱和度为5,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基,所以剩余2个碳原子,取代基可以为:-CH2CH2COOH和-NH2,-CH(COOH)CH3和-NH2,-CH2CH2NH2和-COOH,-CH(NH2)CH3和-COOH,-CH2(NH2)COOH和-CH3,-CH2COOH和-CH2NH2,两个取代基又分为邻、间、对三种,所以同分异构体为6×3=18,故选A.
的不饱和度为5,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基,所以剩余2个碳原子,取代基可以为:-CH2CH2COOH和-NH2,-CH(COOH)CH3和-NH2,-CH2CH2NH2和-COOH,-CH(NH2)CH3和-COOH,-CH2(NH2)COOH和-CH3,-CH2COOH和-CH2NH2,两个取代基又分为邻、间、对三种,所以同分异构体为6×3=18,故选A.
点评 本题主要考查同分异构体的书写,难度中等,注意支链的确定是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 向碘化钾溶液中加入用硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| B. | 在亚硫酸中加入过量的次氯酸钠溶液:H2SO3+ClO-═Cl-+2H++SO42- | |
| C. | 向Ba(OH)2溶液中加入过量NH4HSO4:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+═2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(乙醇)、KOH | B. | 金刚石、MgF2 | C. | H2SO4、Na2SO4 | D. | P4和CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 2.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 2.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 2.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com