

 £¬øĆ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£®
£¬øĆ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£® £®
£® £®
£® ·ÖĪö AµÄ·Ö×ÓŹ½ĪŖC4H9Cl£¬ŗĖ“Ź²ÕńĒāĘ×±ķĆ÷ĘäÖ»ÓŠŅ»ÖÖ»Æѧ»·¾³µÄĒā£¬ŌņAĪŖ£ØCH3£©3CCl£¬ŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ó¦£¬Éś³ÉBĪŖCH2=C£ØCH3£©2£¬B·¢ÉśŠÅĻ¢2ÖŠµÄ·“Ӧɜ³ÉCĪŖ£ØCH3£©2CHCH2OH£¬C·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖ£ØCH3£©2CHCHO£¬DŌŁÓėĒāŃõ»ÆĶ·“Ó¦£¬Ėį»ÆµĆµ½EĪŖ£ØCH3£©2CHCOOH£¬
FµÄ·Ö×ÓŹ½ĪŖC7H8O£¬±½»·ÉĻµÄŅ»ĀČ“śĪļÖ»ÓŠĮ½ÖÖ£¬Ó¦ŗ¬ÓŠ2øö²»Ķ¬µÄ²ąĮ“£¬ĒŅ“¦ÓŚ¶ŌĪ»£¬ŌņFĪŖ £¬ÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀ·¢ÉśČ”“ś·“Ó¦£¬Éś³ÉGĪŖ
£¬ÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀ·¢ÉśČ”“ś·“Ó¦£¬Éś³ÉGĪŖ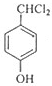 £¬GŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ·¢ÉśĖ®½ā·“Ó¦£¬Ėį»ÆµĆµ½H£¬ÓÉÓŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĮ½øöōĒ»ł²»ĪČ¶Ø£¬Ņ×ĶŃĖ®ŠĪ³ÉōŹ»ł£¬¹ŹHĪŖ
£¬GŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ·¢ÉśĖ®½ā·“Ó¦£¬Ėį»ÆµĆµ½H£¬ÓÉÓŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĮ½øöōĒ»ł²»ĪČ¶Ø£¬Ņ×ĶŃĖ®ŠĪ³ÉōŹ»ł£¬¹ŹHĪŖ £¬HÓėE·¢Éśõ„»Æ·“Ӧɜ³ÉI£¬Ęä·Ö×ÓÖŠŗ¬ÓŠČ©»łŗĶõ„»ł£¬¹ŹIĪŖ
£¬HÓėE·¢Éśõ„»Æ·“Ӧɜ³ÉI£¬Ęä·Ö×ÓÖŠŗ¬ÓŠČ©»łŗĶõ„»ł£¬¹ŹIĪŖ £¬¾Ż“Ė·ÖĪö½ā“š£®
£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗAµÄ·Ö×ÓŹ½ĪŖC4H9Cl£¬ŗĖ“Ź²ÕńĒāĘ×±ķĆ÷ĘäÖ»ÓŠŅ»ÖÖ»Æѧ»·¾³µÄĒā£¬ŌņAĪŖ£ØCH3£©3CCl£¬ŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗ”¢¼ÓČČĢõ¼žĻĀ·¢ÉśĻūČ„·“Ó¦£¬Éś³ÉBĪŖCH2=C£ØCH3£©2£¬B·¢ÉśŠÅĻ¢2ÖŠµÄ·“Ӧɜ³ÉCĪŖ£ØCH3£©2CHCH2OH£¬C·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖ£ØCH3£©2CHCHO£¬DŌŁÓėĒāŃõ»ÆĶ·“Ó¦£¬Ėį»ÆµĆµ½EĪŖ£ØCH3£©2CHCOOH£¬
FµÄ·Ö×ÓŹ½ĪŖC7H8O£¬±½»·ÉĻµÄŅ»ĀČ“śĪļÖ»ÓŠĮ½ÖÖ£¬Ó¦ŗ¬ÓŠ2øö²»Ķ¬µÄ²ąĮ“£¬ĒŅ“¦ÓŚ¶ŌĪ»£¬ŌņFĪŖ £¬ÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀ·¢ÉśČ”“ś·“Ó¦£¬Éś³ÉGĪŖ
£¬ÓėĀČĘųŌŚ¹āÕÕĢõ¼žĻĀ·¢ÉśČ”“ś·“Ó¦£¬Éś³ÉGĪŖ £¬GŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ·¢ÉśĖ®½ā·“Ó¦£¬Ėį»ÆµĆµ½H£¬ÓÉÓŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĮ½øöōĒ»ł²»ĪČ¶Ø£¬Ņ×ĶŃĖ®ŠĪ³ÉōŹ»ł£¬¹ŹHĪŖ
£¬GŌŚĒāŃõ»ÆÄĘĖ®ČÜŅŗ·¢ÉśĖ®½ā·“Ó¦£¬Ėį»ÆµĆµ½H£¬ÓÉÓŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĮ½øöōĒ»ł²»ĪČ¶Ø£¬Ņ×ĶŃĖ®ŠĪ³ÉōŹ»ł£¬¹ŹHĪŖ £¬HÓėE·¢Éśõ„»Æ·“Ӧɜ³ÉI£¬Ęä·Ö×ÓÖŠŗ¬ÓŠČ©»łŗĶõ„»ł£¬¹ŹIĪŖ
£¬HÓėE·¢Éśõ„»Æ·“Ӧɜ³ÉI£¬Ęä·Ö×ÓÖŠŗ¬ÓŠČ©»łŗĶõ„»ł£¬¹ŹIĪŖ £¬
£¬
£Ø1£©AĪŖC£ØCH3£©3Cl£¬¹Ź“š°øĪŖ£ŗC£ØCH3£©3Cl£»
£Ø2£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬DµÄ½į¹¹¼ņŹ½ĪŖ£ØCH3£©2CHCHO£¬Ćū³ĘĪŖ2-¼×»ł±ūČ©£¬
¹Ź“š°øĪŖ£ŗ2-¼×»ł±ūČ©£»
£Ø3£©EĪŖ£ØCH3£©2CHCOOH£¬Ęä·Ö×ÓŹ½ĪŖC4H8O2£¬
¹Ź“š°øĪŖ£ŗC4H8O2£»
£Ø4£©FÉś³ÉGµÄ»Æѧ·½³ĢŹ½ĪŖ £¬øĆ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£¬
£¬øĆ·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£¬
¹Ź“š°øĪŖ£ŗ £»Č”“ś·“Ó¦£»
£»Č”“ś·“Ó¦£»
£Ø5£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬IµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø6£©I£Ø £©µÄĶ¬ĻµĪļJ±ČIĻą¶Ō·Ö×ÓÖŹĮ抔14£¬J±ČIÉŁŅ»øö-CH2-Ō×ÓĶÅ£¬JµÄĶ¬·ÖŅģ¹¹ĢåÖŠÄÜĶ¬Ź±Āś×ćČēĻĀĢõ¼ž£ŗ¢Ł±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£¬¢Ś¼ČÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ÓÖÄÜÓė±„ŗĶNaHCO3ČÜŅŗ·“Ó¦·Å³öCO2£¬ŌņJµÄĶ¬·ÖŅģ¹¹Ģåŗ¬ÓŠ-CHO”¢-COOH£¬
£©µÄĶ¬ĻµĪļJ±ČIĻą¶Ō·Ö×ÓÖŹĮ抔14£¬J±ČIÉŁŅ»øö-CH2-Ō×ÓĶÅ£¬JµÄĶ¬·ÖŅģ¹¹ĢåÖŠÄÜĶ¬Ź±Āś×ćČēĻĀĢõ¼ž£ŗ¢Ł±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»ł£¬¢Ś¼ČÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ÓÖÄÜÓė±„ŗĶNaHCO3ČÜŅŗ·“Ó¦·Å³öCO2£¬ŌņJµÄĶ¬·ÖŅģ¹¹Ģåŗ¬ÓŠ-CHO”¢-COOH£¬
²ąĮ“ĪŖ-CHO”¢-CH2CH2COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
²ąĮ“ĪŖ-CHO”¢-CH£ØCH3£©COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
²ąĮ“ĪŖ-CH2CHO”¢-CH2COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
²ąĮ“ĪŖ-CH2CH2CHO”¢-COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
²ąĮ“ĪŖ-CH£ØCH3£©CHO”¢-COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
²ąĮ“ĪŖ-CH3”¢-CH£ØCHO£©COOH£¬ÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĪ»ÖĆ£¬
¹Ź·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ6”Į3=18ÖÖ£¬
JµÄŅ»øöĶ¬·ÖŅģ¹¹Ģå·¢ÉśŅų¾µ·“Ó¦²¢Ėį»ÆŗóŗĖ“Ź²ÕńĒāĘ×ĪŖČż×é·å£¬ĒŅ·åĆ껿±ČĪŖ2£ŗ2£ŗ1£¬¶ųJµÄĶ¬·ÖŅģ¹¹Ģå·¢ÉśŅų¾µ·“Ó¦²¢Ėį»ÆŗóµÄ²śĪļ±½»·²ąĮ“ÖĮÉŁÓŠ2ÖÖHŌ×Ó£¬¹Ź²śĪļÖŠ±½»·ÉĻÖ»ÓŠ1ÖÖHŌ×Ó£¬²śĪļÓŠ2øö-COOH£¬Ó¦»¹ŗ¬ÓŠ2øö-CH2-£¬2øö²ąĮ“ĻąĶ¬ĒŅ“¦ÓŚ¶ŌĪ»£¬²śĪļÖŠ²ąĮ“ĪŖ-CH2COOH£¬¹Ź·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ18£» £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶʶĻ¼°ÖŖŹ¶ĒØŅĘÄÜĮ¦£¬øł¾ŻÄ³Š©ĪļÖŹ·Ö×ÓŹ½”¢·“Ó¦Ģõ¼ž¼°ĢāøųŠÅĻ¢½ųŠŠĶʶĻ£¬£Ø6£©ÖŠĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“ŹĒŅדķµć”¢ÄŃµć£¬ĢāÄæÄѶČÖŠµČ£®


 µć¾¦ŠĀ½Ģ²ÄČ«Äܽā¶ĮĻµĮŠ“š°ø
µć¾¦ŠĀ½Ģ²ÄČ«Äܽā¶ĮĻµĮŠ“š°ø Š”ѧ½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
Š”ѧ½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬½į¹¹¼ņŹ½H2C=CH2£®
£¬½į¹¹¼ņŹ½H2C=CH2£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ¼×ŹĒŅŅĻ© | B£® | ŅŅæÉÄÜŹĒĘĻĢŃĢĒ | ||
| C£® | ±ūŅ»¶ØŹĒCH3CH2X £ØXŹĒĀ±ĖŲŌ×Ó£© | D£® | ¶”Ź®H2”śŅŅ“¼µÄ·“Ó¦ŹōÓŚ¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź¹ÓĆ18.4 mol•L-1µÄĮņĖį | B£® | ÉżøßČÜŅŗµÄĪĀ¶Č | ||
| C£® | ĻņČÜŅŗÖŠ¼ÓČėÉŁĮæĻõĖį | D£® | °ŃŠæ·Ū»»³ÉŠææé£Øʬ£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
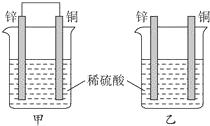
| A£® | Į½ÉÕ±ÖŠČÜŅŗµÄpHÖµ¾łŌö“ó | B£® | ²śÉśĘųÅŻµÄĖŁĀŹ¼×±ČŅŅæģ | ||
| C£® | Į½ÉÕ±ÖŠĶʬ±ķĆę¾łĪŽĘųÅŻ²śÉś | D£® | ¼×ÖŠĶʬŹĒÕż¼«£¬ŅŅÖŠŠæʬŹĒøŗ¼« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 H2”¢CH3OHŹĒÓÅÖŹµÄĒå½ąČ¼ĮĻ£¬æÉÖĘ×÷Č¼ĮĻµē³Ų£®
H2”¢CH3OHŹĒÓÅÖŹµÄĒå½ąČ¼ĮĻ£¬æÉÖĘ×÷Č¼ĮĻµē³Ų£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com