
A、B、D、E为原子序数依次增大的短周期元素。A、B组成的气体甲能使湿润的红色石蕊试纸变蓝;A、D处于同一主族,E的最外层电子数等于其电子层数。
(1)B在元素周期表的位置是??? ???? ?? ;四种元素的简单离子,半径最大的是????? (填离子符号);单质D暴露于空气中最终产物是?? ????? ???????? 。
(2)B的一种氧化物BO2与水反应的化学方程式为:????????????????????????????? 。
(3)甲和B的最高价氧化物的水化物反应生成乙。在0.1 mol·L-1乙溶液中,所含离子浓度由大到小的顺序是????????????????????????????????????????????????????????????? 。
(4)25℃时,E的最高价氧化物的水化物KSP=1.0×10-34,使含0.1 mol·L-1E离子的溶液开始产生沉淀的pH为?????????????? 。
(1)第二周期VA族(1分 );N3-(2分 ); Na2CO3 (2分 )
(2)3NO2 + H2O == 2HNO3 + NO(2分 )
(3)c(NO3-)>c(NH4+)>c(H+)>c(OH-)(2分 )??????????? (4)3(2分 )
【解析】
试题分析:A、B、D、E为原子序数依次增大的短周期元素。A、B组成的气体甲能使湿润的红色石蕊试纸变蓝,该气体是氨气,则A是氢元素,B是氮元素;A、D处于同一主族,且D的原子序数大于氮元素,所以D是钠元素;E的最外层电子数等于其电子层数,E是第三周期元素,所以E是铝元素。
(1)氮元素在元素周期表的位置是第二周期VA族;离子的电子层数越大,离子半径越大,在核外电子排布相同的条件下,原子序数越大,离子半径越小,因此四种元素的简单离子,半径最大的是N3-;钠是活泼的金属,极易与水、氧气反应,生成的氢氧化钠吸收二氧化碳变为碳酸钠,所以金属钠暴露于空气中最终产物是Na2CO3。
(2)氮元素的一种氧化物NO2与水反应的化学方程式为3NO2 + H2O=2HNO3 + NO。
(3)甲和B的最高价氧化物的水化物反应生成乙,则乙应该是硝酸铵。溶液中NH4+水解溶液显酸性,因此在0.1 mol·L-1乙溶液中,所含离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-)。
(4)根据氢氧化铝的溶度积常数表达式KSP= c(Al3+)·c3(OH-)可知,要使含0.1 mol·L-1铝离子的溶液开始产生沉淀,则溶液的c(OH-)最小值为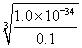 =1×10-11mol/L,则氢离子浓度是1×10-3mol/L,所以pH=3。
=1×10-11mol/L,则氢离子浓度是1×10-3mol/L,所以pH=3。
考点:考查元素推断、物质结构与性质的综合应用


科目:高中化学 来源:高考三人行 化学 题型:043
已知某化合物甲,分子中只含C、H、O三种元素,其C、H的质量分数合计为78.4%.又已知甲分子中有1个碳原子,它的4个价键分别连接在4个不同的原子(或原子团)上,如图所示.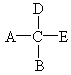
A、B、D、E为互不相同的原子或原子团.
(1)写出甲的分子式.(2)写出甲的结构式.
查看答案和解析>>
科目:高中化学 来源:活题巧解巧练·高考化学(第一轮) 题型:043
已知某化合物甲,分子中只含C,H,O三种元素,其C,H的质量分数合计为78.4%.又已知,甲分子中有一个碳原子,它的4个价键分别连接4个不同的原子(或原子团),如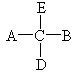 .其中A,B,D,E为互不相同的原子或原子团.
.其中A,B,D,E为互不相同的原子或原子团.
(1)建议甲的分子式为________.
(2)写出甲的结构简式,并以系统命名法对其命名为________.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
已知某化合物甲,分子中只含C、H、O三种元素,其C、H的质量分数合计为78.4%又已知甲分子中有一个碳原子,它的4个价键分别连接在4个不同的原子(或原子团)上,如图所示.A、B、D、E为互不相同的原子或原子团.
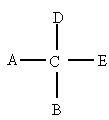
(1)写出甲的分子式.
(2)写出甲的结构简式.
查看答案和解析>>
科目:高中化学 来源: 题型:
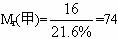 ,A、B、D、E为互不相同的原子或原子团。试分析甲的分子式应为_________,写出甲的结构简式并用系统命名法命名。
,A、B、D、E为互不相同的原子或原子团。试分析甲的分子式应为_________,写出甲的结构简式并用系统命名法命名。查看答案和解析>>
科目:高中化学 来源:2015届四川省广安市高一下学期期末考试化学试卷(解析版) 题型:填空题
已知A、E是生活中常见的两种有机物;B是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平;A能在酸性高锰酸钾的条件下生成E; C是高分子化合物。在一定条件下由A可以转变为有机物B、C、D、E、F(A、B、D、E碳原子数相等)。转变关系如下:


请回答下列问题:
(1)B的电子式是____________。
(2) E的官能团名称是____________。
(3) 写出实现下列转化的化学方程式
①A→D
② B→C
(4) A是一种高效、低耗、污染小的可再生的清洁能源,已知1molA完全燃烧生成CO2气体和水蒸气放出1367kJ热量,则在相同条件下,1molA完全燃烧生成CO2气体和液态水,放出的热量________ 1367kJ(填“>”、“=”或“<”)。
(5) 在可逆反应当中,产率指的是某种生成物的实际产量与理论产量的比值.若100克A和120克E反应生成了88克F,则F的产率是____________(用百分数表示)
(6)下列关于A、B、C、D、E、F六种物质说法正确的是____________
A.C具有固定的元素组成,因而有固定的熔沸点
B.C中有不饱和键,所以能使高锰酸钾溶液褪色
C. 取等物质的量的B和C完全燃烧后,生成的CO2和H2O的物质的量分别相等
D.由B生成C是通过加聚反应制得的
E. 分别燃烧1molA和B生成CO2和H2O的耗氧气量,其中A和B耗氧量相等
F.在 A+E→ F转变中,有含氧的小分子生成,小分子的氧原子来至于A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com