
| A. | 某无色透明的酸性溶液:Cl-、Na+、MnO4-、SO42- | |
| B. | 含CO32-的溶液:K+、Na+、AlO2-、Cl- | |
| C. | 能使pH试纸变深蓝色的溶液:Na+、NH4+、K+、CO32- | |
| D. | 由水电离产生的c(H+)=10-12mol/L的溶液:K+、I-、Cl-、NO3- |
分析 A.高锰酸根离子为有色离子;
B.四种离子之间不反应,都不与碳酸根离子反应;
C.该溶液中存在大量氢氧根离子,铵根离子与氢氧根离子反应;
D.该溶液呈酸性或碱性,溶液中存在大量氢离子或氢氧根离子.
解答 解:A.MnO4-为有色离子,在溶液中不能大量共存,故A错误;
B.K+、Na+、AlO2-、Cl-之间不反应,都不与CO32-反应,在溶液中能够大量共存,故B正确;
C.能使pH试纸变深蓝色的溶液呈碱性,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.由水电离产生的c(H+)=10-12mol/L的溶液呈酸性或碱性,I-、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题

| 步骤① | 在5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色 |
| 步骤② | 往5mL重新配制的5mL1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色较短时间内溶液颜色变为浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1.6 g O2和O3混合气体中原子总数为0.1NA | |
| B. | 标准状况下,过氧化钠与水反应生成1.12 L氧气时转移电子数目为0.2NA | |
| C. | 0.1 mol•L的CH3COONa溶液中CH3COOH和CH3COO-总数为0.1NA | |
| D. | 常温常压下,4 g He中,含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

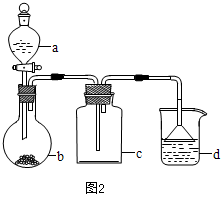
| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A1Cl3 | B. | Na2O | C. | Na(Al(OH)4) | D. | SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、N可能位于同一周期 | B. | M、N不可能位于同一主族 | ||
| C. | M、N可能形成共价化合物MN | D. | M、N可能形成离子化合物MN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO+2HCl═CuCl2+H2O | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | Zn+H2SO4═ZnSO4+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先生成沉淀,后沉淀全部溶解 | |
| B. | 当溶液中Ba2+全部沉淀出来时,沉淀的总物质的量最大 | |
| C. | 最后得到的沉淀是BaSO4 | |
| D. | 最后的沉淀为2 mol BaSO4、1 mol Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 序号 | 现象 | 结论 |
| I | B装置中黑色氧化铜变为红色 | 反应生成了Cu或Cu2O |
| II | C装置中无水CuSO4变蓝 | 反应生成了H2O |
| III | E装置中收集到无色无味气体 | 反应生成了N2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com