
【题目】硫酸锰铵晶体可用作织物和木材加工的防火剂等。由二氧化锰等作原料制取硫酸锰铵晶体步骤如下:
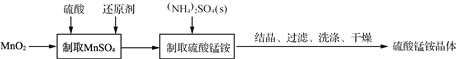
(1)实验前,需称量MnO2的质量,这是因为____________________________。
(2) “制取MnSO4”时,可用C6H12O6(葡萄糖)、H2C2O4(草酸)等物质作还原剂。
①用C6H12O6作还原剂(被氧化为CO2)时,发生反应的n(MnO2)/n(C6H12O6)=________。
②用H2C2O4作还原剂,发生反应的化学方程式为____________________________。
(3)一种测定硫酸锰铵晶体[设为: (NH4)xMny(SO4)z·wH2O]组成的方法如下:
①称取一定量的硫酸锰铵晶体配成250 mL溶液A。
②取25.00 mL溶液A加入足量的BaCl2溶液得BaSO4 0.512 6 g。
③另取25.00 mL溶液A加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min[4NH![]() +6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
+6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
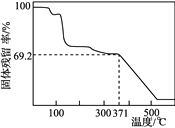
④取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在371 ℃时已完全失去结晶水)。根据以上实验数据计算确定硫酸锰铵晶体的化学式(写出计算过程)。__________________
【答案】 确定制备硫酸锰铵时应加入硫酸、还原剂及(NH4)2SO4的质量 12 MnO2 +H2C2O4+H2SO4===MnSO4+2CO2↑+2H2O n(SO![]() ) =n(BaSO4) =
) =n(BaSO4) =![]() =2.200×10-3 mol,NH
=2.200×10-3 mol,NH![]() ) =n(NaOH)=0.100 0 mol·L-1×22.00 mL×10-3 L·mL-1=2.200×10-3 mol,(Mn2+)=
) =n(NaOH)=0.100 0 mol·L-1×22.00 mL×10-3 L·mL-1=2.200×10-3 mol,(Mn2+)=![]() [2 n(SO
[2 n(SO![]() )-n(NH
)-n(NH![]() )]=1.100×10-3 mol,x∶y∶z=2∶1∶2,化学式为(NH4)2Mn(SO4)2·wH2O,
)]=1.100×10-3 mol,x∶y∶z=2∶1∶2,化学式为(NH4)2Mn(SO4)2·wH2O,![]() =69.2% w=7,化学式为(NH4)2Mn(SO4)2·7H2O
=69.2% w=7,化学式为(NH4)2Mn(SO4)2·7H2O
【解析】(1)实验前需要称量MnO2的质量,以确定应加入硫酸、还原剂及(NH4)2SO4的质量;
(2) ①用C6H12O6作还原剂(被氧化为CO2)时,根据电子转移守恒可推出,Mn降低2价,C升高6×4价,所以发生反应的n(MnO2)/n(C6H12O6)=12;②用H2C2O4作还原剂时,反应的化学方程式为MnO2+H2C2O4+H2SO4=MnSO4+2CO2↑+2H2O
(3)根据BaSO40.5126g可得n(SO42-)=n(BaSO4)= ![]() =2.200×10-3mol,n(NH4+)= n(NaOH) = 0.1000mol·L-1×22.00mL×10-3L·mL-1=2.200×10-3mol,由电荷守恒可得n(Mn2+)=
=2.200×10-3mol,n(NH4+)= n(NaOH) = 0.1000mol·L-1×22.00mL×10-3L·mL-1=2.200×10-3mol,由电荷守恒可得n(Mn2+)= ![]() [2n(SO42-)- n(NH4+)]=1.100×10-3mol,所以x:y:z =2:1:2,设该物质的化学式为(NH4)2Mn(SO4)2·wH2O,则由图象可得
[2n(SO42-)- n(NH4+)]=1.100×10-3mol,所以x:y:z =2:1:2,设该物质的化学式为(NH4)2Mn(SO4)2·wH2O,则由图象可得 ![]() = 69.2% w=7,化学式为(NH4)2Mn(SO4)2·7H2O。
= 69.2% w=7,化学式为(NH4)2Mn(SO4)2·7H2O。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】在标准状况下,一个充满Cl2的恒容密闭容器的质量为74.6 g,若改充满N2,其质量为66 g,则容器的容积为:
A.5.6LB.11.2LC.2.24LD.4.48L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、SO42—、NH4+、CO32—、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____,可能存在的离子有______;
(2)原溶液中c(CO32—)为____,c(NH4+)____c(SO42—) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl)__c(SO42—) (填“>、<或=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4和0.2 mol H2S,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如下图所示:
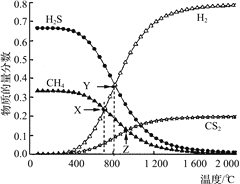
下列说法正确的是( )
A. 该反应的ΔH<0
B. X点CH4的转化率为20%
C. X点与Y点容器内压强比为51∶55
D. 维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1 mol时v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是 ( )
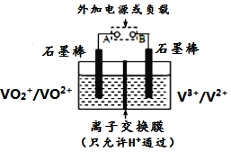
A. 放电时,右槽电解液pH不变
B. 充电时,阴极电解液pH升高
C. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
D. 充电时,每转移1mol电子,右槽中n(H+)的变化量为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫氰酸盐、苯酚及硫代硫酸盐是HPF脱硫废液中的主要污染物(其中还含有Cl-、SO![]() 、Na+等),可用NaClO3、H2SO4作脱除的试剂。
、Na+等),可用NaClO3、H2SO4作脱除的试剂。
(1)Cl2与热的NaOH溶液反应生成NaClO3,该反应的化学方程式为____________________________。
(2) 常温时,反应C6H5O-+H2O ![]() C6H5OH+OH-的平衡常数为K=________(C6H5OH的Ka=1×10-10)。
C6H5OH+OH-的平衡常数为K=________(C6H5OH的Ka=1×10-10)。
(3)处理该废水需经预处理和再处理阶段。
①用浓硫酸对600 mL HPF脱硫废液进行酸化预处理(反应温度100℃),其结果如表1所示:
表1 预处理前后三种离子浓度变化情况
项目 | S2O | SCN-(g·L-1) | 苯酚(g·L-1) | pH |
处理前 | 34.28 | 70.11 | 1.3 | 8.55 |
处理后 | 0.91 | 69.76 | 1.35 | 2.4 |
由表1可知,该处理过程中主要被除去的污染物是________。
②对预处理后废液进行再处理(反应温度100 ℃)时,13次依次向废液中加入试剂情况如表2所示:
表2 13次依次加入试剂情况
次数 | 1 | 2 | 3 | 4 | span>5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
NaClO3/g | 16.3 | 0 | 0 | 0 | 0 | 0 | 7.6 | 0 | 5.7 | 0 | 10.9 | 0 | 7.1 |
浓H2SO4/mL | 0 | 2 | 2 | 2 | 4 | 4 | 0 | 4 | 0 | 4 | 0 | 4 | 0 |
实验结果如图1所示:
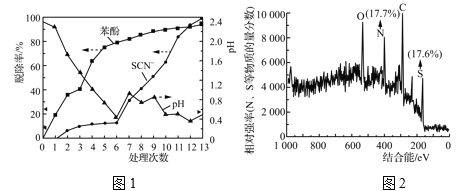
前![]() 和Cl-反应产生Cl2有关。该白色沉淀可能的结构简式为______________。
和Cl-反应产生Cl2有关。该白色沉淀可能的结构简式为______________。
③由表2和图1中数据得出,第7~13次操作中SCN-在较强酸性条件下被ClO![]() (不水解)氧化的依据是________。此过程中产生大量砖红色沉淀(夹杂少量白色沉淀),对沉淀进行XPS分析,部分元素的物质的量分数如图2所示。已知SCN-可被某些氧化剂(如Cu2+等)最终氧化为砖红色的沉淀(SCN)x。一种推测认为该实验中产生的砖红色沉淀为(SCN)x,支持该推测的证据有:________。
(不水解)氧化的依据是________。此过程中产生大量砖红色沉淀(夹杂少量白色沉淀),对沉淀进行XPS分析,部分元素的物质的量分数如图2所示。已知SCN-可被某些氧化剂(如Cu2+等)最终氧化为砖红色的沉淀(SCN)x。一种推测认为该实验中产生的砖红色沉淀为(SCN)x,支持该推测的证据有:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用元素周期律解释的是( )
A. 热稳定性:Na2CO3>NaHCO3 B. 酸性:H2CO3>H2SiO3
C. 碱性:NaOH>LiOH D. 热稳定性:HF>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类赖以生存与发展的重要物质基础。
(1)普通玻璃的主要成分是Na2SiO3、CaSiO3和___(填化学式)。用于汽车或火车车窗的玻璃是___玻璃。
(2)在复合材料由两部分组成,,一部分作___,另一部分作______,如_____就是一种复合材料。
(3)硅酸盐水泥的主要成分是_______, 为调节水泥的硬化速度,常在水泥中加入___。
(4)工业上制水泥和玻璃需用到的共同原料是______,制水泥和陶瓷需用到的共同原料是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为Na3AlF6 ,其中含有_______________________________等化学键。
(2)生成物中含有10个电子的分子是________(写分子式),该分子的空间构型_______,中心原子的杂化方式为___________________。
(3)反应物中所含元素电负性最大的元素为________(填元素符号),写出其原子最外层的电子排布图:_______________,它的氢化物的沸点比同主族其它氢化物的沸点高,原因是:_______________________________。
(4)冰晶石由两种微粒构成,它的晶胞结构如图甲所示,小黑点“●”位于大立方体的顶点和面心,小圆圈“○”位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处小三角“”所代表的是__________(填“小黑点”或“小圆圈”),它代表的是______________(填微粒化学式)。
(5)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
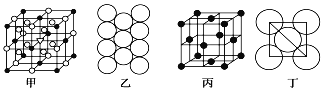
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为___________个; Al晶体的密度为__________(用字母表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com