
| A�� | ��֪C��ʯī��s��=C�����ʯ��s����H��O������ʯ��ʯī�ȶ� | |
| B�� | ��֪2H2��g��+O2��g���T2H20��1����H=-571.6kJ•mol-1����������ȼ����Ϊ-285.8kJ•mol-1 | |
| C�� | ��20.0 gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ�����������������ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��NaOH��aq��+CH3COOH��aq���TH3COOHNa��aq��+H2O��l��H=-57.4kJ•mol-1 | |
| D�� | ��֪2C��s��+2O2��g��=2CO2��g����H1��2C��s��+O2��g���T2CO��g����H2 ���H1����H2 |
���� A�����ʵ�����Խ��Խ���ȶ�������Խ��Խ�ȶ���
B��ȼ������ָ1mol��������ȫȼ�������ȶ���������ų���������
C������Ϊ���ᣬ�����������������ϡ��Һ��1mol�������������Ʒ�Ӧ�ų�������С��1molNaOH��HCl��Ӧ�ų���������
D�����ݸ�˹���ɿɵã�2CO��g��+O2��g��=2CO2��g����H=��H1-��H2��COȼ��Ϊ���ȷ�Ӧ��
��� �⣺A��ʯīת��Ϊ���ʯʱ��Ҫ����������˵�����ʯ��������ʯī������Խ��Խ�ȶ�������ʯī�Ƚ��ʯ�ȶ�����A����
B����2H2��g��+O2��g��=2H2O��l����H=-571.6 kJ/mol����֪1mol������ȫȼ�������ȶ���������ų�������Ϊ285.8KJ������������ȼ���ȡ�H=-285.8 kJ/mol����B��ȷ��
C��20.0g NaOH���ʵ���Ϊ0.5mol��NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ����������1mol����������ȫ�кͷ���57.4KJ��������������ڵ���ƽ�⣬������������ȹ��̣�ϡ�����ϡNaOH��Һ��Ӧ����С��57.4kJ����C����
D�����ݸ�˹���ɿɵã�2CO��g��+O2��g��=2CO2��g����H=��H1-��H2��COȼ��Ϊ���ȷ�Ӧ������H1-��H2��0�����H1����H2����D����
��ѡB��
���� ���⿼���Ȼ�ѧ����ʽ��ȼ���ȡ��к��ȡ���Ӧ�ȴ�С�Ƚϵȣ��ѶȲ���ע��Ը�������⡢��˹���ɵ�Ӧ�ã�


 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| X | X+������Neԭ����ͬ�ĵ��Ӳ�ṹ |
| Y | �����������Ǵ�����һ�룬���������������۵ľ���ֵ��� |
| Z | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
| T | Ԫ�ص��ʵ���ɫ�ǻ���ɫ������ |
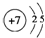 ��
��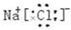 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0 | B�� | 1 | C�� | 2 | D�� | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
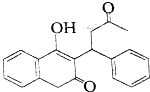
 �����Ƶ�A�Ĺ���ʽ���á�*���������̼ԭ�ӣ�����ϵͳ������������
�����Ƶ�A�Ĺ���ʽ���á�*���������̼ԭ�ӣ�����ϵͳ�������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A��Cl2��CH4ȡ����Ӧ��IJ�� | 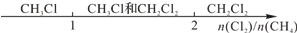 |
| B�����ռ�Һ��ͨ��SO2��IJ�� | 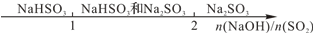 |
| C������ϡ���ᷴӦ�� | 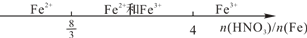 |
| D����AlCl3��Һ�еμ�NaOH��Һ����Ԫ�صĴ�����ʽ�� | 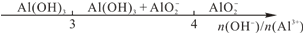 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������SO2ͨ�뺬Fe2+��Cl-��Ba2+��Al3+����Һ�У������������ܴ������� | |
| B�� | ��NaClO��Һ��ͨ������������̼�����ӷ���ʽ��2ClO-+CO2+H2O�T2HClO+CO32- | |
| C�� | ����������������HBr��Һ��Ӧ�����ӷ���ʽ��Fe��OH��2+3H+�TFe2++3H2O | |
| D�� | ��100mL1mol•L-1��FeCl3��Һ������NaS�����ַ�Ӧ�����ɳ���10.4g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
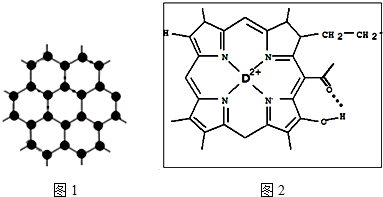
| A�� | M���кܸߵ��۷е� | |
| B�� | M����������������������� | |
| C�� | M�ɱ���Ϊͬ�������� | |
| D�� | M����Cԭ�Ӻ�Oԭ�Ӱ�1��2�ı�������ɵ�ƽ����״�ľ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
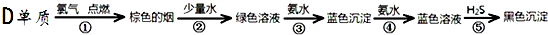
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H4=��H1+��H3-��H2 | B�� | ��H4=��H1+2��H3-��H2 | ||
| C�� | ��H4=��H2+��H1+2��H3 | D�� | ��H4=2����H2-��H1+2��H3�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com