
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:____与盐酸反应最剧烈;_________与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律
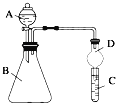
(3)仪器B的名称为_____,干燥管D的作用为_______。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C______的现象,即可证明,从环境保护的观点考虑,此装置缺少尾气处理装置,可用_____溶液吸收尾气。
(5)若要证明非金属性:N>C>Si,则在A中加硝酸、B中加碳酸钙,并在两装置间加一个除去挥发出来的HNO3的装置,C中加_____溶液观察到C中溶液白色沉淀,即可证明。
【答案】钾 铝 S2﹣+Cl2═S↓+2Cl﹣ 锥形瓶 防止倒吸 溶液变蓝色 NaOH 硅酸钠
【解析】
根据金属性强弱分析反应剧烈程度;根据非金属性强弱分析实验原理及实验现象;根据提供的实验装置及氧化还原反应原理对非金属性强弱比较进行探究性实验。
Ⅰ.(1)反应速率由反应物的性质决定,金属性越强,与酸反应越剧烈,所以钾与盐酸反应最剧烈;相同物质的量的金属,铝失电子数最多,所以与盐酸反应生成的气体最多;
(2)Na2S与氯气反应生成硫和氯化钠,氯气为氧化剂,硫为氧化产物,所以氯气的氧化性强于硫,可证明Cl的非金属性比S强,反应的离子方程式为S2﹣+Cl2═S↓+2Cl﹣;
Ⅱ.(3)如图所示仪器B的名称为锥形瓶;根据图示,干燥管中没有干燥剂,而一端插入溶液,所以干燥管D的作用为防止倒吸;
(4)B中生成的氯气可以置换出碘化钾中的碘,淀粉遇碘变蓝,所以观察到C中的现象为溶液变蓝色;过量的氯气有毒,所以应该用NaOH进行尾气处理;
(5)若要证明非金属性:N>C>Si,则需证明它们最高价氧化物的水化物酸性:硝酸>碳酸>硅酸,利用强酸制弱酸的原理加以证明,B装置中产生二氧化碳气体,说明硝酸的酸性强于碳酸,将除去硝酸蒸气后的二氧化碳气体通入C中的硅酸钠溶液,生成难溶的硅酸,则说明碳酸酸性强于硅酸,故答案为: 硅酸钠。


科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为![]() )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体(![]() )的工艺流程如下所示:
)的工艺流程如下所示:

下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的![]() 应回收利用
应回收利用
C. 通入氯气的目的是氧化![]()
D. 用![]() 制取无水
制取无水![]() 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_______;
(2)写出氮气分子的结构式______。
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩C2H6,含有极性键和非极性键的是_____;(填序号)
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦ 碘升华;⑧溴蒸气被木炭吸附。
(1)未破坏化学键的是____;(填序号)
(2)仅离子键被破坏的是___。(填序号)
Ⅳ.下列物质:①1H、2H、3H;②H2O、D2O、T2O;③O2、O3;④14N、14C
(1)互为同位素的是:_____;(填序号)
(2)互为同素异形体的是:____;(填序号)
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N、Ga元素因其在生产、生活和科研领域的重要作用而备受关注。
请回答下列问题:
(1)基态Ga原子中含有___________________种能量不同的电子,其中能量最高的电子的电子云轮廓图的形状为_________________________。
(2)Ga单质有晶体和玻璃体两种形态,区别二者最可靠的科学方法为_____________________。
(3)Ga分别与N、P、AS形成化合物的晶体结构与金刚石相似,其熔点如下表所示:
物质 | GaN | GaP | GaAs |
熔点/℃ | 1700 | 1465 | 1238 |
①从结构的角度分析,三种晶体熔点不同的原因为____________________________________。
②GaN晶体中含有的化学键类型为______________(填选项字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.氢键
③GaP的晶胞结构可看作金刚石晶胞内部的碳原子被P原子代替,顶点和面心的碳原子被Ga原子代替。若GaP晶体的密度为pg·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为____________nm。
(4)第二周期元素中,基态原子的第一电离能大于基态氮原子的有__________种。
(5)NaNH2是一种重要的工业原料。
①钠元素的焰色反应为黄色。很多金属元素能产生焰色反应的微观原因为___________________。
②NH2-中氮原子的杂化方式为_____________;该离子的空间构型为________________。
③写出与NH2-互为等电子体的分子的化学式:____________________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯是重要的有机化工原料,以甲苯为原料,制备香料、药物中间体(M)和高分子化合物(N)的一种合成路线如下:

已知:R1CHO+R2CH2CHO![]()
![]()
![]()
![]() (R1、R2表示氢原子或烃基)。
(R1、R2表示氢原子或烃基)。
请回答下列问题:
(1)B中官能团的名称为______________________,E的化学名称为____________________。
(2)H→N的反应类型为_______________________________。
(3)G分子中最多有________个碳原子共平面。顺式-N的结构简式为_____________________。
(4)C+D→M的化学方程式为_________________________________________。
(5)同时满足下列条件的H 的同分异构体有___________种(不考虑立体异构)。
①苯环上连接2个取代基
②能发生银镜反应,且1mol最多生成4molAg
(6)参照上述合成路线和信息,写出以甲醇和乙醛为原料(无机试剂任选),设计制备![]() 的合成路线:______________________________________________。
的合成路线:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M为原子序数依次增大的短周期元素,周期表中X原子半径最小,Y元素形成化合物种类最多,Z元素的氢化物水溶液呈碱性,常温下L可以形成两种液态氢化物,M的最高价氧化物对应的水化物呈两性。回答下列问题:
(1)L元素形成单质的名称为______;M在元素周期表中的位置为____;五种元素的原子半径从大到小的顺序是______(用元素符号表示)。
(2)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为______。
(3)写出由X、Z、L三种元素组成的离子化合物与稀的NaOH溶液加热反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。
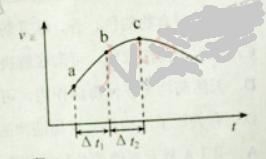
A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过下列两步实验测定草酸晶体(H2C2O4·xH2O)中结晶水x的值:
①称取2.52 g草酸晶体,配制成100 .00 mL溶液。
②取25.00 mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为0.100 mol·L-1 KMnO4溶液进行滴定。其反应原理是:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
请回答下列问题:
(1)实验②中,KMnO4应装在______滴定管中(填“酸式”、“碱式”)。
(2)如图表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积______。
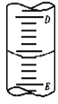
A.是amL B.是(50-a)mL
C.一定大于amL D.一定大于(50-a)mL
(3)判断达到滴定终点的现象是_____________________________;
若滴定终点时,共用去KMnO4溶液20.00 mL,则x =__________。
(4)若在滴入KMnO4溶液之前滴定管的尖嘴部分有气泡,滴定结束后气泡消失,则会使测定结果______(偏高、偏低或无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z、R 原子序数依次增大。由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体。金属单质Z在空气中燃烧生成的化合物可与水发生反应生成气体。下列说法正确的是
A. 简单离子的半径: X < Z < R
B. X的简单氢化物比Y的稳定
C. a、b、c中均含有极性共价健,且 a属于电解质,b和c都属于非电解质
D. W、X、Y、R四种元素形成的化合物一定会促进水的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com