
 ij»ÆѧŠĖȤŠ”×飬ÄāĢ½¾æŗĶ±Č½ĻSO2ŗĶ Cl2µÄĘư׊Ō£¬Éč¼ĘČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖƶžĢ×£®ĒėÄć²ĪÓėĢ½¾æ²¢»Ų“šĻĀĮŠĪŹĢā£®
ij»ÆѧŠĖȤŠ”×飬ÄāĢ½¾æŗĶ±Č½ĻSO2ŗĶ Cl2µÄĘư׊Ō£¬Éč¼ĘČēĶ¼ĖłŹ¾µÄŹµŃé×°ÖƶžĢ×£®ĒėÄć²ĪÓėĢ½¾æ²¢»Ų“šĻĀĮŠĪŹĢā£®·ÖĪö £Ø1£©øł¾ŻSO2½įŗĻÓŠ»śÉ«ĖŲŠĪ³É²»ĪȶØĪŽÉ«ĪļÖŹ£¬¼ÓČČŗó»Öø“ŌĄ“µÄŃÕÉ«£»
£Ø2£©øł¾ŻCl2ŗĶĖ®·“Ӧɜ³É¾ßÓŠĒæŃõ»ÆŠŌµÄ“ĪĀČĖį£¬“ĪĀČĖįµÄĘÆ°××÷ÓĆ²»æÉ»Öø“£»
£Ø3£©ÓÉ£Ø1£©ŗĶ£Ø2£©µĆ³öÕżČ·½įĀŪ£»
£Ø4£©øł¾ŻCl2µÄĘÆ°×ŌĄķ£»
£Ø5£©øł¾ŻCl2ÓŠ¶¾£¬Ó¦½ųŠŠĪ²Ęų“¦Ąķ£»
½ā“š ½ā£ŗ£Ø1£©SO2½įŗĻÓŠ»śÉ«ĖŲŠĪ³É²»ĪȶØĪŽÉ«ĪļÖŹ£¬¼ÓČČŗó»Öø“ŗģÉ«£»
¹Ź“š°øĪŖ£ŗ»Öø“£»
£Ø2£©Cl2ŗĶĖ®·“Ӧɜ³É“ĪĀČĖį£¬“ĪĀČĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬ĘäĘÆ°××÷ÓĆ²»æÉ»Öø“£»
¹Ź“š°øĪŖ£ŗ²»»Öø“£»
£Ø3£©ÓÉ£Ø1£©ŗĶ£Ø2£©æÉÖŖ£¬SO2ŗĶC12µÄĘÆ°×ŌĄķ²»ĻąĶ¬£»
¹Ź“š°øĪŖ£ŗ²»ĻąĶ¬£»
£Ø4£©Cl2ÓėĖ®·“Ӧɜ³É“ĪĀČĖį£¬“ĪĀČĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬ÄÜÓĆÓŚĘÆ°×£»
¹Ź“š°øĪŖ£ŗHClO£»
£Ø5£©Cl2ÓŠ¶¾£¬æÉĶعżNaOHČÜŅŗĪüŹÕ£»
¹Ź“š°øĪŖ£ŗ³żČ„ƻӊ·“Ó¦µÄCl2£®
µćĘĄ ±¾Ģāæ¼²éĮĖ“ĪĀČĖįŗĶ¶žŃõ»ÆĮņµÄĘư׊Ō£¬ÄŃ¶Č²»“ó£¬×¢Ņā“ĪĀČĖįµÄĘư׊ŌŹĒÓĄ¾ĆŠŌµÄ£¬¶žŃõ»ÆĮņµÄĘư׊ŌŹĒŌŻŹ±µÄ£¬ĘäĘÆ°×ŌĄķŅ²²»Ķ¬£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»¹ÜŹ²Ć“·“Ó¦Ź¹ÓĆ“ß»Æ¼Į£¬¶¼æÉŅŌ¼Óæģ·“Ó¦ĖŁĀŹ | |
| B£® | æÉÄę·“Ó¦A£Øg£©?B£Øg£©+C£Øg£©£¬Ōö“óŃ¹Ēæ£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹŌö“ó | |
| C£® | ¶Ō“ļµ½Ę½ŗāµÄŅ»øö·ÅČȵÄæÉÄę·“Ó¦£¬Čō½µĪĀ£¬ŌņÕż·“Ó¦ĖŁĀŹ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹŌö“ó | |
| D£® | ²Ī¼Ó·“Ó¦µÄĪļÖŹµÄŠŌÖŹŹĒ¾ö¶Ø»Æѧ·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 £¬“ĖČ²ĢžæÉÄܵĽį¹¹ÓŠ£Ø””””£©
£¬“ĖČ²ĢžæÉÄܵĽį¹¹ÓŠ£Ø””””£©| A£® | 1ÖÖ | B£® | 2ÖÖ | C£® | 3ÖÖ | D£® | 4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĻ”ŃĪĖįĻ“µÓŹ¢·Å¹żŹÆ»ŅĖ®µÄŹŌ¼ĮĘæ | |
| B£® | ÅäÖĘFeCl3ČÜŅŗŹ±£¬ĻņČÜŅŗÖŠ¼ÓČėÉŁĮæFeŗĶĻ”ŃĪĖį | |
| C£® | ÓĆ“ż²āŅŗČóĻ“µĪ¶ØÓƵÄ׶ŠĪĘæ | |
| D£® | Na2CO3ČÜŅŗ±£“ęŌŚ“ų²£Į§ČūµÄŹŌ¼ĮĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Čō·“Ó¦Ź±ŠĪ³ÉŠĀ»Æѧ¼üŹĶ·ÅµÄÄÜĮæ“óÓŚ¶ĻĮŃ¾É»Æѧ¼üĖłĪüŹÕµÄÄÜĮ棬ŌņøĆ»Æѧ·“Ó¦ŹĒŹĶ·ÅÄÜĮæµÄ·“Ó¦ | |
| B£® | Čō·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬ŌņøĆ»Æѧ·“Ó¦ĪŖŹĶ·ÅÄÜĮæµÄ·“Ó¦ | |
| C£® | »Æѧ·“Ó¦ÖŠÄÜĮæ±ä»ÆµÄ“óŠ”Óė·“Ó¦ĪļµÄÖŹĮæ¶ąÉŁĪŽ¹Ų | |
| D£® | »Æѧ·“Ó¦±ŲČ»°éĖę×ÅÄÜĮæµÄ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 20% | B£® | 25% | C£® | 50% | D£® | 75% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé²½Öč | ŹµŃéĻÖĻó |
| 1£®½«Ć¾ĢõÓĆÉ°Ö½“ņÄ„ŗ󣬷ÅČė·ŠĖ®ÖŠ£»ŌŁĻņČÜŅŗÖŠµĪ¼Ó·ÓĢŖČÜŅŗ | A£®ø”ŌŚĖ®ĆęÉĻ£¬ČŪ³ÉŠ”Ēņ£¬×ö²»¶ØĻņŌĖ¶Æ£¬ĖęÖ®ĻūŹ§£¬ČÜŅŗ±ä³ÉŗģÉ«£® |
| 2£®ĻņŠĀÖʵƵÄNa2SČÜŅŗÖŠµĪ¼ÓÉŁĮæŠĀÖʵÄĀČĖ® | B£®ÓŠĘųĢå²śÉś£¬ČÜŅŗ±ä³ÉĒ³ŗģÉ« |
| 3£®½«Ņ»Š”æ齚ŹōÄĘ·ÅČėµĪÓŠ·ÓĢŖČÜŅŗµÄĄäĖ®ÖŠ | C£®¾ēĮŅ·“Ó¦£¬ŃøĖŁ²śÉś“óĮæĪŽÉ«ĘųĢ壮 |
| 4£®½«Ć¾ĢõĶ¶ČėĻ”ŃĪĖįÖŠ | D£®·“Ó¦²»Ź®·Ö¾ēĮŅ£¬²śÉśĪŽÉ«ĘųĢå |
| 5£®½«ĀĮĢõĶ¶ČėĻ”ŃĪĖįÖŠ | E£®Éś³Éµ»ĘÉ«³Įµķ |
| ŹµŃéÄŚČŻ | ŹµŃéĻÖĻó | Ąė×Ó·½³ĢŹ½ |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
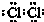 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5øöCl2 | B£® | 1øöClŌ×Ó | ||
| C£® | 3.01”Į1023øöClŌ×Ó | D£® | 6.02”Į1023øöClŌ×Ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com