
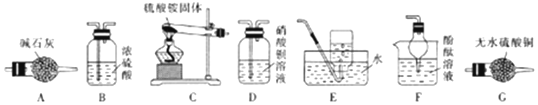
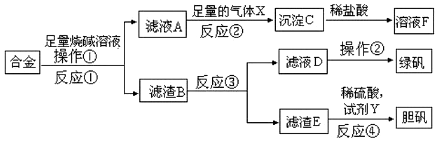
·ÖĪö £Ø1£©AŅĒĘ÷Ćū³ĘĪŖøÉŌļ¹Ü£¬¹ĢĢå¼ÓČČÉś³ÉµÄĖ®µ¹Į÷ČŻŅ×ŅżĘšÕØĮŃŹŌ¹Ü£»
£Ø2£©¢ŁÖ¤Ć÷Ė®Éś³ÉµÄŹŌ¼ĮĪŖĪŽĖ®ĮņĖįĶ£¬Óöµ½Ė®±äĄ¶É«£¬BÖŠÅØĮņĖįĪüŹÕ°±Ęų£»
¢Ś¼ģŃé°×É«³ĮµķŹĒBaSO4»¹ŹĒBaSO3£¬æÉŅŌ¼ÓČėĖį¹Ū²ģŹĒ·ńČܽāÅŠ¶Ļ£»
¢Ū¶žŃõ»ÆĮņĶØČėĻõĖį±µČÜŅŗÖŠĪö³öĻ”ĻõĖįÄÜŃõ»Æ¶žŃõ»ÆĮņĪŖĮņĖį£¬ĻõĖį±µ±»»¹ŌĪŖŅ»Ńõ»ÆµŖ£»
¢Ü¼××éĶ¬Ń§Éč¼Ę·½°ø£ŗC”śG”śB”śD”śE¹ż³ĢæÉŅŌ¼ģŃéÉś³ÉµÄ¶žŃõ»ÆĮņ”¢Ė®ŗĶµŖĘų£»
£Ø3£©·Ö½āÉś³ÉµÄĘųĢåĶعż¼īŹÆ»ŅĪüŹÕ¶žŃõ»ÆĮņ£¬ĶØČė×°ÖĆFÖŠ£¬ČōČÜŅŗ±äŗģÉ«Ö¤Ć÷ÓŠ°±ĘųµÄÉś³É£»
£Ø4£©ŅĄ¾ŻĮņĖįøłĄė×ÓŹŲŗć¼ĘĖć£»
½ā“š ½ā£ŗ£Øl£©A×°ÖĆŹ¢×°¼īŹÆ»ŅµÄŅĒĘ÷ŹĒøÉŌļ¹Ü£¬3£ØNH4£©2SO4$\frac{\underline{\;\;”÷\;\;}}{\;}$4NH3”ü+3SO2”ü+N2+6H2O£¬C×°ÖĆÖŠ¼ÓČČ·Ö½ā£¬²śĪļÖŠÓŠĖ®Éś³É“óŹŌ¹ÜĻņĻĀĒ抱µÄŌŅņŹĒ£ŗѳʷ·Ö½āÉś³ÉĮĖĖ®£¬·ĄÖ¹ŹŌ¹ÜÕØĮŃ£¬
¹Ź“š°øĪŖ£ŗøÉŌļ¹Ü£»ŃłĘ··Ö½āÉś³ÉĮĖĖ®£¬·ĄÖ¹ŹŌ¹ÜÕØĮŃ£»
£Ø2£©¢ŁÄÜÖ¤Ć÷ÓŠĖ®Éś³ÉµÄŹµŃéĻÖĻóŹĒG×°ÖĆÖŠ°×É«·ŪÄ©±ä³ÉĄ¶É«£¬B×°ÖƵÄ×÷ÓĆŹĒĪüŹÕ°±Ęų£¬
¹Ź“š°øĪŖ£ŗG×°ÖĆÖŠ°×É«·ŪÄ©±ä³ÉĄ¶É«£»ĪüŹÕ°±Ęų£»
¢ŚŹµŃéÖŠ£¬¹Ū²ģµ½D×°ÖĆÖŠ²śÉś°×É«³Įµķ£®ŹµŃéĶź±Ļŗ󣬹żĀĖD×°ÖĆÖŠ»ģŗĻĪļµĆ°×É«³Įµķ£®ĪŖĮĖ¼ģŃé°×É«³ĮµķŹĒBaSO4»¹ŹĒBaSO3£¬ŹµŃé·½°øÉč¼ĘĪŖ£ŗȔɣĮæ°×É«³ĮµķÓŚŹŌ¹Ü£¬µĪ¼Ó×ćĮæŃĪĖį£¬Čō°×É«³ĮµķČܽā£¬ŌņŹĒBaSO3£¬·“Ö®ŌņŹĒBaSO4£¬
¹Ź“š°øĪŖ£ŗȔɣĮæ°×É«³ĮµķÓŚŹŌ¹Ü£¬µĪ¼Ó×ćĮæŃĪĖį£¬Čō°×É«³ĮµķČܽā£¬ŌņŹĒBaSO3£¬·“Ö®ŌņŹĒBaSO4£»
¢Ū¶žŃõ»ÆĮņĶØČėĻõĖį±µČÜŅŗÖŠĪö³öĻ”ĻõĖįÄÜŃõ»Æ¶žŃõ»ÆĮņĪŖĮņĖį£¬ĻõĖį±»»¹ŌĪŖŅ»Ńõ»ÆµŖ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ3Ba2++2NO3-+3SO2+2H2O=3BaSO4”ż+2NO+4H+£¬
¹Ź“š°øĪŖ£ŗ3Ba2++2NO3-+3SO2+2H2O=3BaSO4”ż+2NO+4H+£»
¢Ü¼××éĶ¬Ń§Éč¼Ę·½°ø£ŗC”śG”śB”śD”śE£¬¹ĢĢåŌŚCÖŠ·Ö½āÉś³ÉµÄĘųĢåĶعżG¼ģŃéĖ®µÄÉś³É£¬Ķعż×°ÖĆBĪüŹÕ°±Ęų£¬Ķعż×°ÖĆD¼ģŃ鶞Ńõ»ÆĮņµÄÉś³É£¬Ķعż×°ÖĆEÅŠ¶ĻÉś³É²»ČÜÓŚĖ®µÄ°±Ęų£¬¹ż³ĢæÉŅŌ¼ģŃéÉś³ÉµÄ¶žŃõ»ÆĮņ”¢Ė®ŗĶµŖĘų£¬
¹Ź“š°øĪŖ£ŗH2O”¢SO2”¢N2£»
£Ø3£©¢Ł·Ö½āÉś³ÉµÄĘųĢåĶعż¼īŹÆ»ŅĪüŹÕ¶žŃõ»ÆĮņ£¬ĶØČė×°ÖĆFÖŠ£¬ČōČÜŅŗ±äŗģÉ«Ö¤Ć÷ÓŠ°±ĘųµÄÉś³É£¬ĘųĢå“Ó×óÖĮÓŅ£¬×°ÖĆĮ¬½ÓĖ³ŠņĪŖC”¢A”¢F£¬
¹Ź“š°øĪŖ£ŗA”¢F£»
¢ŚÄÜÖ¤Ć÷ÓŠ°±ĘųÉś³ÉµÄŹµŃéĻÖĻóŹĒĪŽÉ«·ÓĢŖČÜŅŗ±äŗģ£¬
¹Ź“š°øĪŖ£ŗĪŽÉ«·ÓĢŖČÜŅŗ±äŗģ£»
£Ø4£©Č”15.0gѳʷČÜÓŚÕōĮóĖ®£¬¼ÓČė×ćĮæĀČ»Æ±µČÜŅŗŗĶĻ”ŃĪĖį£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘÖŲ£¬BaSO4ÖŹĮæĪŖ23.3g£¬ĪļÖŹµÄĮæ=$\frac{23.3g}{233g/mol}$=0.1mol£¬
øĆѳʷ֊ĮņĖįļ§µÄÖŹĮæ·ÖŹż=$\frac{0.1mol”Į132g/mol}{15.0g}$”Į100%=88%£¬
¹Ź“š°øĪŖ£ŗ88%£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹŠŌÖŹµÄŹµŃéŃéÖ¤·½·Ø”¢¼ģŃéŹŌ¼ĮŃ”Ōń”¢Ö÷ŅŖŹĒ×°ÖƵÄ×÷ÓĆŗĶĮ¬½Ó£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2-¼×»ł¶”ĶéŅ²³ĘŅģ¶”Ķé | |
| B£® | 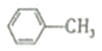 µÄ-äå“śĪļŗĶ µÄ-äå“śĪļŗĶ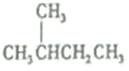 µÄŅ»äå“śĪļ¶¼ÓŠ4Ö֣ز»æ¼ĀĒĮ¢ĢåŅģ¹¹£© µÄŅ»äå“śĪļ¶¼ÓŠ4Ö֣ز»æ¼ĀĒĮ¢ĢåŅģ¹¹£© | |
| C£® | ĶéĢž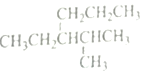 µÄĆüĆūŹĒ£ŗ3-Ņģ±ū»ł¼ŗĶé µÄĆüĆūŹĒ£ŗ3-Ņģ±ū»ł¼ŗĶé | |
| D£® | 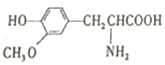 Óė Óė 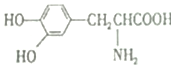 »„ĪŖĶ¬ĻµĪļ »„ĪŖĶ¬ĻµĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆĪļ | B£® | ĮņĖįŃĪ | C£® | ĻõĖįŃĪ | D£® | Ģ¼ĖįŃĪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ü | B£® | ¢Ł¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | Č«²æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
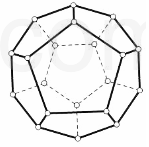 2000 Äź£¬µĀ¹śFreiburg“óѧµÄH£®PrinzbachŠū³Ę£¬ĖūĆĒĶعżÕŖ³ż·Ø£¬ŅŃ¾ŌŚĘųĻąÖŹĘ×ŅĒµÄĘųĢåÖŠ·¢ĻÖĮĖ×īŠ”µÄĒņĢ¼·Ö×Ó£Øø»ĄÕĻ©£©--C20£ØČēĶ¼ĖłŹ¾£©£®Č»ŗóŌŚµē×Ó³å»÷ÖŹĘ×ŅĒÖŠ¹Ū²ģµ½ĮĖĪ¢ĮæC20+ŗĶC202+µÄ“ęŌŚ£® Ėū½«C20H20 ČܽāŌŚŅŗäåĄļ£¬ŌŚÉÕĘæĄļ¼ÓŃ¹³¤Ź±¼ä»ŲĮ÷£¬×īÖÕµĆµ½Ę½¾ł×é³ÉĪŖ C20HBr13µÄ²śĪļ£®
2000 Äź£¬µĀ¹śFreiburg“óѧµÄH£®PrinzbachŠū³Ę£¬ĖūĆĒĶعżÕŖ³ż·Ø£¬ŅŃ¾ŌŚĘųĻąÖŹĘ×ŅĒµÄĘųĢåÖŠ·¢ĻÖĮĖ×īŠ”µÄĒņĢ¼·Ö×Ó£Øø»ĄÕĻ©£©--C20£ØČēĶ¼ĖłŹ¾£©£®Č»ŗóŌŚµē×Ó³å»÷ÖŹĘ×ŅĒÖŠ¹Ū²ģµ½ĮĖĪ¢ĮæC20+ŗĶC202+µÄ“ęŌŚ£® Ėū½«C20H20 ČܽāŌŚŅŗäåĄļ£¬ŌŚÉÕĘæĄļ¼ÓŃ¹³¤Ź±¼ä»ŲĮ÷£¬×īÖÕµĆµ½Ę½¾ł×é³ÉĪŖ C20HBr13µÄ²śĪļ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “×ĖįČÜŅŗÓėŠĀÖĘĒāŃõ»ÆĶ·“Ó¦£ŗ2H++Cu£ØOH£©2”śCu2++2H2O | |
| B£® | Äį²“½šĖįÓėĢ¼ĖįĒāÄĘ·“Ó¦£ŗ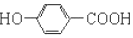 +2HCO3-”ś +2HCO3-”ś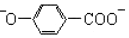 +2CO2”ü+2H2O +2CO2”ü+2H2O | |
| C£® | ±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĢ¼£ŗC6H5O-+CO2+H2O”śC6H5OH+HCO3- | |
| D£® | ¼×Č©ČÜŅŗÓė×ćĮæµÄŅų°±ČÜŅŗ¹²ČČ£ŗHCHO+2[Ag£ØNH3£©2]++2OH$\stackrel{”÷}{”ś}$CO32-+2NH4++2Ag”ż+2NH3+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com