
| A. | KCl | B. | K2S | C. | Na2S | D. | Na2O |
科目:高中化学 来源: 题型:选择题
| 选项 | 分子式 | 同分异构体数目 |
| A | C4H8O2 | 1 |
| B | C6H12O2 | 2 |
| C | C8H16O2 | 3 |
| D | C10H20O2 | 4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
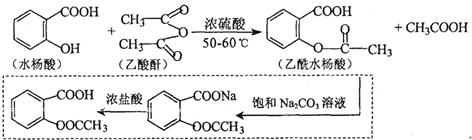
 .
. .
.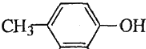 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用PH试纸可测得某溶液的pH为6.5 | |
| B. | 可用25mL碱式滴定管量取20.00mLKMnO4溶液 | |
| C. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 | |
| D. | 把CO中毒的病人放入高压氧仓中解毒,其原理符合勒夏特列原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+CuSO4=FeSO4+Cu | B. | Cl2+H2O=HCl+HClO | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | AgNO3+HCl=AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 共价键 | H-H | N≡N | H-N |
| 键能(kJ•mol-1) | 436 | 945 | 391 |
| 装置 | 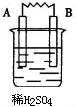 | 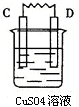 | 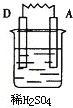 | 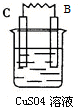 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 | 金属B不断溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .化合物
.化合物 是合成药物的中间体,请写出以有机物A和
是合成药物的中间体,请写出以有机物A和 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com