
在周期表主族元素中,甲元素与乙、丙、丁三元素紧密相邻(上下或左右),甲、乙两元素的原子序数之和等于丙元素的原子序数,这四种元素原子的最外层电子数之和为20。下列说法正确的是( )
A.甲、乙、丙、丁四种元素均为短周期元素
B.气态氢化物的稳定性:甲>乙
C.最高价氧化物对应的水化物的酸性:甲<丙
D.元素丁与乙形成的化合物中可能含有离子键
科目:高中化学 来源: 题型:
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现。某种兴奋剂的结构简式如下:
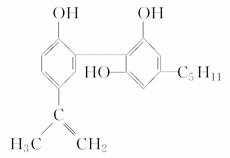
关于它的说法正确的是
( )
A.它的化学式为C19H26O3
B.从结构上看,它属于酚类
C.从结构上看,它属于醇类
D.从元素组成上看,它可以在氧气中燃烧生成CO2和水
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)游泳池水中的含氯气量应该控制在0.5 mg·L-1至1.0 mg·L-1之间,写出氯气溶于水的化学方程式
________________________________________________________________________。
溶于水后产生的________可杀菌消毒。
(2)下图显示一星期中每天19时时泳池水中的氯气含量,哪几天使用泳池不安全________________________________________________________________________。
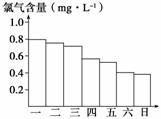
(3)你认为哪几天的天气火热、阳光强烈________,说出一种理由是______________。
(4)若把一片紫色的花瓣放入氯水中,可观察到的现象是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示:
| 阳离子 | NH |
| 阴离子 | OH-、NO |
取等质量的三种化合物配制相同体积的溶液,其溶 质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④
C.③⑤ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4 + 6Na2O2===2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑
①该反应中的氧化剂是________,还原剂是________,每生成1 mol Na2FeO4转移________mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用__________________________________
________________________________________________________________________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO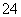 、Cl-、H2O。
、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:____________________________
________________________________________________________________________。
②每生成1 mol FeO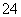 转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙===丁+己,甲+丙===戊+己; 0.1 mol·L-1丁溶液的pH为13(25 ℃)。下列说法正确的是( )
A.原子半径:W>Y>Z>X
B.Y元素在周期表中的位置为第3周期第ⅣA族
C.1 mol甲与足量的乙完全反应共转移1 mol电子
D.化合物甲中只有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见( )
A. NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为:NH4HCO3+HCl===NH4Cl+CO2↑+H2O ΔH=+Q
查看答案和解析>>
科目:高中化学 来源: 题型:
1体积气态烃和2体积氯化氢恰好完全发生反应后,其产物最多还能和8体积氯气发生取代反应,由此可以推断原气态烃是(气体体积均在相同条件下测定)( )
A.乙炔 B.1,3-丁二烯 C.戊炔 D.丙炔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com