
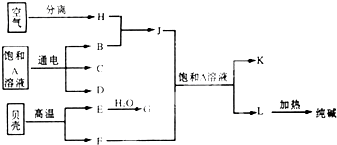
 以海水中常见的物质A为原料可以发展很多种工业,如图中包含了几种基本工业生产,请根据各物质之间的转化关系.回答下列问题:
以海水中常见的物质A为原料可以发展很多种工业,如图中包含了几种基本工业生产,请根据各物质之间的转化关系.回答下列问题:| 水 |
| 溶解 |
| 过量BaCl2溶液 |
| 过滤 |
| 水 |
| 洗涤 |
| 低温烘干、冷却、称重 |
| ng |
| 197g/mol |
| n |
| 197 |
| n |
| 197 |
| 106n |
| 197 |
| ||
| m |
m-
| ||
| m |
m-
| ||
| m |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、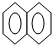 +HNO3 +HNO3
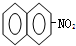 +H2O +H2O | |||
B、
| |||
C、2CH3CH2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
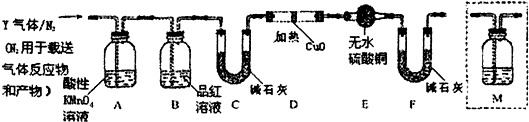
| ① | ② | ③ | |
| 硫酸溶液体积/mL | 50 | 50 | 50 |
| 称取铁钉质量/g | 5.0 | 6.0 | 7.0 |
| 再投入铜粉质量/g | 1.0 | 1.0 | 1.0 |
| 标准状况下的体积/L | 1.97 | 2.24 | 2.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:

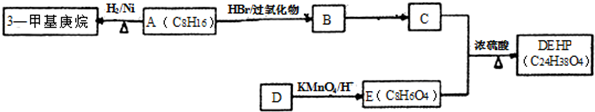
 消去HCl后的产物记为F,写出两种F的能发生银镜反应、且只含3种不同化学环境氢原子的同分异构体的结构简式.
消去HCl后的产物记为F,写出两种F的能发生银镜反应、且只含3种不同化学环境氢原子的同分异构体的结构简式.查看答案和解析>>
科目:高中化学 来源: 题型:

| 催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com