
| A、①②③ | B、①②④ |
| C、②③ | D、①②③④ |


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、可用湿润的淀粉碘化钾试纸检验产物Q |
| B、K2FeO4在水中的电离方程式为K2FeO4═2K++Fe6++4O2一 |
| C、反应中氧化剂与还原剂的物质的量之比为1:8 |
| D、反应中涉及的6种物质均为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
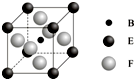 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液中可能大量存在Al3+、NH4+、Cl?、S2? |
| B、室温时,c(H+)=1×10-13mol/L的溶液中可能大量存在Mg2+、Cu2+、SO42-、NO3- |
| C、0.1mol/LNH4HCO3溶液中可能大量存在K+、Na+、NO3-、Cl- |
| D、中性溶液中可能大量存在Na+、Ca2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、还原剂是HCl,氧化剂是MnO2 |
| B、每生成1molCl2,转移电子的物质的量为2mol |
| C、每消耗1mol MnO2,起还原剂作用的HCl消耗2mol |
| D、标准状况下生成11.2L Cl2,转移电子的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
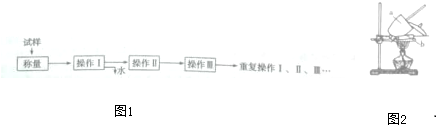
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
| A、四种溶液中,Na2CO3溶液中水的电离程度最大 |
| B、NaHSO3溶液显酸性的原因是:NaHSO3=Na++H++SO32- |
| C、向氯水中加入少量NaHCO3(s),可以增大氯水中次氯酸的浓度 |
| D、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| ③ | 向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、可能含有的离子是①②⑦ |
| B、肯定含有的离子是①④ |
| C、不能确定的离子是①③⑦ |
| D、肯定没有的离子是②⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com