
| 实验装置 | 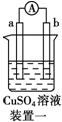 | 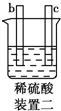 | 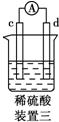 |  |
| 部分实验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
| A. | a>b>c>d | B. | b>c>d>a | C. | d>a>b>c | D. | a>b>d>c |
分析 装置一:发生电化学腐蚀,活泼金属作负极,不活泼金属作正极,负极发生氧化反应,负极质量减少;
装置二:发生化学腐蚀,活泼金属与酸反应放出氢气,不活泼金属与酸不反应;
装置三:发生电化学腐蚀,正极有气泡;
装置四:发生电化学腐蚀,氢离子的正极上得电子发生还原反应生成氢气.
解答 解:装置一:发生电化学腐蚀,a极质量减小,b极质量增加,a极为负极,b极为正极,所以金属的活动性顺序a>b;
装置二:发生化学腐蚀,b极有气体产生,c极无变化,所以金属的活动性顺序b>c;
装置三:发生电化学腐蚀,d极溶解,所以d是负极,c极有气体产生,所以c是正极,所以金属的活动性顺序d>c;
装置四:发生电化学腐蚀,电流从a极流向d极,a极为正极,d极为负极,所以金属的活动性顺序d>a;
所以这四种金属的活动性顺序d>a>b>c,
故选C.
点评 本题主要考查了金属的活动性,注意从原电池的角度比较金属性的活动性顺序,注意金属活动性的比较方法的积累,题目难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;其燃烧含碳产物的结构式为:O=C=O;CH4与Cl2生成CCl4的化学方程式CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
;燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;其燃烧含碳产物的结构式为:O=C=O;CH4与Cl2生成CCl4的化学方程式CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
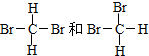 (在横线上填相应的序号)
(在横线上填相应的序号)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
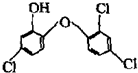 据报道,高露洁牙膏中含有的消毒剂三氯生遇含氯自来水能生成哥罗芳(三氯甲烷),哥罗芳能导致肝病甚至癌症,已知三氯生的结构简式如图所示,有关说法正确的是( )
据报道,高露洁牙膏中含有的消毒剂三氯生遇含氯自来水能生成哥罗芳(三氯甲烷),哥罗芳能导致肝病甚至癌症,已知三氯生的结构简式如图所示,有关说法正确的是( )| A. | 三氯生的分子式为:C12H6Cl3O2 | |
| B. | 哥罗芳存在同分异构体 | |
| C. | 1mol三氯生最多能与4molNaOH溶液反应 | |
| D. | 三氯生遇FeCl3溶液显紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com