
A、沸点的高低: |
| B、熔点:SiO2>CsCl>CBr4>CF4 |
| C、硬度:镁>铝>镁铝合金 |
| D、水溶性:HF>Br2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
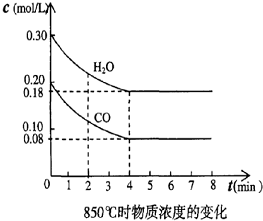 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,且K=1.
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,且K=1.| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯材料化学稳定性好,所以容易产生白色污染 |
| B、蚕丝制品和棉花制品可以通过灼烧的方法加以鉴别 |
| C、糖类、油脂、蛋白质一定条件下都能发生水解反应 |
| D、可用新制Cu(OH)2悬浊液检验尿液中是否含有葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe-3e-=Fe3+ |
| B、O2+2H2O+4e-=4OH- |
| C、Fe-2e-=Fe2+ |
| D、O2+2H2O-4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
| B、H2O、CH3COOH、CaCO3均含有氧元素,都是氧化物 |
| C、HCl、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D、HNO3、浓硫酸都具有强氧化性,都是氧化性酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 异常情况 | 可能的原因 |
| ① | 蒸发结晶时,蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到蒸发皿底部 |
| ② | 粗盐水过滤后,滤液仍浑浊 | 滤纸与漏斗内壁间有气泡 |
| ③ | 萃取时,振荡溶液,静置不分层 | 萃取剂加得太多 |
| ④ | 蒸馏时,发现冷凝管破裂 | 没有通冷凝水或先加热后通冷凝水 |
| A、①②③④ | B、②③④ |
| C、②③ | D、② |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2013年5月23日广东省食品安全委员会公布了抽检发现的120批次镉超标大米,再次拉响了食品安全警报.下列“镉大米”(隔的元素符号Cd)的说法正确的是( )
2013年5月23日广东省食品安全委员会公布了抽检发现的120批次镉超标大米,再次拉响了食品安全警报.下列“镉大米”(隔的元素符号Cd)的说法正确的是( )| A、大米中含有超标的可溶性Cr2O32-或CrO42- |
| B、土壤中重金属镉离子(Cd2+)严重超标,稻米对于镉吸附作用造成污染 |
| C、大米中的淀粉与镉反应生成了更具毒性的化学物质 |
| D、可以用多次清洗的办法除去“镉大米”中的镉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该物质分子式为K3C60 |
| B、K3C60的摩尔质量是837 |
| C、1molK3C60中含有的离子键的数目为63×6.02×1023个 |
| D、K3C60中既有离子键,又有共价键,在熔融状态下能导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com