
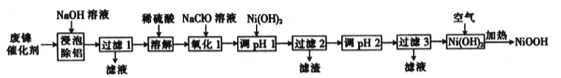
����Ŀ����ʽ������(NiOOH)�����������ص��������ϣ����÷�����������Ҫ��Ni��A1������Cr��FeS��)���Ʊ����乤���������£�
�ش��������⣺
��1�������ݳ�����ʱ��������Ӧ�Ļ�ѧ����ʽΪ________________��
��2�����ܽ⡱ʱ�ų�������Ϊ_________���ѧʽ)��
��3��������1��ʱ�����������£���Һ�е�Fe2+������ΪFe3+�������ӷ���ʽΪ______________��
��4����֪�������½������ӿ�ʼ��������ȫ������pH���±���
��ʼ������pH | ��ȫ������pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
����pH 1��ʱ����ҺpH��ΧΪ__________������2���������ijɷ�Ϊ___________(�ѧʽ)��
��5��д���ڿ����м���Ni(OH)2��ȡNiOOH�Ļ�ѧ����ʽ______________��
��6�������Ȳ���֣����Ƶõ�NiOOH�л����Ni(OH)2������ɿɱ�ʾΪxNiOOH��y Ni(OH)2���ֳ�ȡ8.29g xNiOOH��y Ni(OH)2��Ʒ����ϡ���ᣬ��������Һ���壬������200mL,������ȡ20.00 mL,��0.010mol��L-1��KMnO4����Һ�ζ����ظ���������2�Σ�ƽ������KMnO4 ����Һ 20.00 mL����֪ 5Ni2++MnO4-+8H+=5Ni3++Mn2++4H2O����x=_________��y=_________��
���𰸡� 2Al+2NaOH+2H2O=2NaAlO2+3H2�� H2�� H2S 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O 5.66.2 Cr(OH)3�� Fe(OH)3 4Ni(OH)2+O2![]() 4NiOOH+2H2O 8 1
4NiOOH+2H2O 8 1
��������(1)�����ݳ�����ʱ���������ƽ����ܽ⣬��Ӧ�Ļ�ѧ����ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2�����ʴ�Ϊ��2Al+2NaOH+2H2O=2NaAlO2+3H2����
(2)���ܽ���ʱ��������Ni��Cr��FeS��Ӧ���ų�������ΪH2�� H2S���ʴ�Ϊ��H2�� H2S��
(3)������1��ʱ�����������£��������ƽ���Һ�е�Fe2+������ΪFe3+�����ӷ���ʽΪ2Fe2++ClO-+2H+=2Fe3++Cl-+H2O���ʴ�Ϊ��2Fe2++ClO-+2H+=2Fe3++Cl-+H2O��
(4)���ݽ������ӿ�ʼ��������ȫ������pH��������pH 1��ʱ��Ŀ���ǽ�Fe3+��Cr3+��ȥ�������ҺpH��ΧΪ5.66.2������2���������ijɷ�ΪCr(OH)3�� Fe(OH)3���ʴ�Ϊ��5.66.2��Cr(OH)3�� Fe(OH)3��
(5)�ڿ����м���Ni(OH)2��ȡNiOOH�Ļ�ѧ����ʽΪ4Ni(OH)2+O2![]() 4NiOOH+2H2O���ʴ�Ϊ��4Ni(OH)2+O2
4NiOOH+2H2O���ʴ�Ϊ��4Ni(OH)2+O2![]() 4NiOOH+2H2O��
4NiOOH+2H2O��
(6)����KMnO4���ʵ�����0.01 molL-1��0.02L=2��10-4 mol������5Ni2++MnO4-+8H+=5Ni3++Mn2++4H2O��֪����Ʒ�к��е�Ni2+���ʵ�����2��10-4 mol��5��(200��20)=0.01 mol��0.01 mol��Ni(OH)2������Ϊ93g/mol��0.01 mol=0.93g����NiOOH������Ϊ8.29g-0.93g=7.36g�����ʵ���Ϊ![]() =0.08mol��x��y=n(NiOOH)��n[Ni(OH)2]=0.08 mol��0.01 mol=8��1����x=8��y=1���ʴ�Ϊ��8��1��
=0.08mol��x��y=n(NiOOH)��n[Ni(OH)2]=0.08 mol��0.01 mol=8��1����x=8��y=1���ʴ�Ϊ��8��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵ�������һ�����������Ĺ�沥�úܻ�,��������ʹ��ʱ,��һ��ɫҺ�����ij������,����װ�������ĺ���,�����������͡��������ڡ���,�dz����㡣�����Ʋ�����ʺ���ɫҺ�������( )��
A.����狀�ˮ B.Ũ�����ˮ
C.�����ƺ�ˮ D.����ƾ���ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѹǿ��ѹ�������������ƽ�����ƶ�
A. ����Ӧ�����ƶ� B. �淴Ӧ�����ƶ�
C. ���������������ķ��� D. ��������������ٵķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25���������Һ�У�������ǿ����( )
A. pH = 11����Һ B. c(OH��) = 0.12 mol/L����Һ
C. 1L�к���4 g NaOH����Һ D. c(H+) = 1��10��10 mol/L����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ����Ʒ��ʹ�û�����������У���ȷ����( )
A. �ú�ɫʯ����ֽ������Һ������
B. ����ƿ����ȷŨ�ȵ���Һ����������Ϊ��Ӧ����ʹ��
C. ����ϡ����ʱ,�����ձ���ע��Ũ���ᣬ�ټ�ˮϡ��
D. ����NaOH����ʱ����NaOHֱ�ӷ��������ϵ�ֽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��ζ������ɫ����ʳƷ���Ӽ���������Խ��Խ��
B. �߲ˡ�ˮ��������ʳ��ά�����������������彡��
C. άţ��C������������Ҫ���ܣ�ά����c������ˮ
D. ��������������Ԫ�أ�ʳ�ε���Ҫ�ɷ���KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ľ��й���ҵ����2016��12��11���ڱ����佱������Ŀ֮һΪ���Ҽ�һ�����ҩ�������ᰣ��������з������Ĺؼ��м���G��һ�ֺϳ�·�����£�
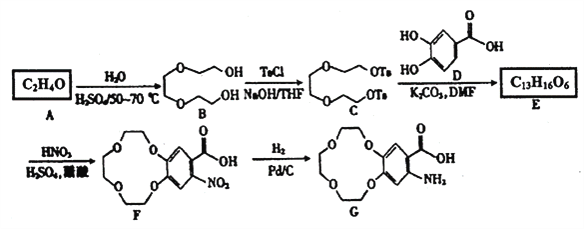
��֪����A������ֻ��һ�ֻ�ѧ�������⣻
��TsClΪ![]() ��
��
��1��A������Ϊ______________��
��2��G�����������ŵ�������______________�� E�Ľṹ��ʽΪ___________________��
��3����B����C�ķ�Ӧ������_____________����F����G�ķ�Ӧ������______________��
��4��PEO����A�����������¼Ӿ۶��ɵ������{���ӣ��üӾ۷�Ӧ�Ļ�ѧ����ʽΪ_______________��
��5����ȡ�������廯����W��D��ͬ���칹�塣W���ܷ���������Ӧ��ˮ�ⷴӦ��������FeCl3��Һ������ɫ��Ӧ��1molW������4molNaOH��Ӧ��W�ĺ˴Ź�������ֻ��4��塣W�Ľṹ��ʽΪ_________________��
��6�����������ϳ�·��, ���������ױ���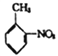 �����Ҵ�Ϊԭ�ϣ����Լ���ѡ��������Ʊ��ڰ���������������
�����Ҵ�Ϊԭ�ϣ����Լ���ѡ��������Ʊ��ڰ���������������![]() ���ĺϳ�·�ߡ�_________________
���ĺϳ�·�ߡ�_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������Һ�е���Ũ�ȵĹ�ϵ��ȷ����
A. pH��4��CH3COOH��Һ�У���ˮ���������c��H������1.0��10��4mol��L��1
B. ���ʵ���Ũ����ȵĢ٣�NH4��2SO3��Һ�͢�NH4HSO4��Һ�е�c��![]() �����٣���
�����٣���
C. pH��3��0.1mol��L��1NaHC2O4��Һ�У�![]()
D. 0.1mol��L��1��Na2CO3��Һ�У�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A. ����TiCl4Ũ��Һ�Ʊ�TiO2��xH2O��Ti4������x��2��H2O![]() TiO2��xH2O��4H��
TiO2��xH2O��4H��
B. ��NH4��2Fe��SO4��2��Һ�м�������KOH��Һ��![]()
C. ��������������ʴʱ��������Ӧ��O2��4H����4e����2H2O
D. ����KI��Һ��ͨ��O2��4H����2I����O2��2H2O��I2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com