
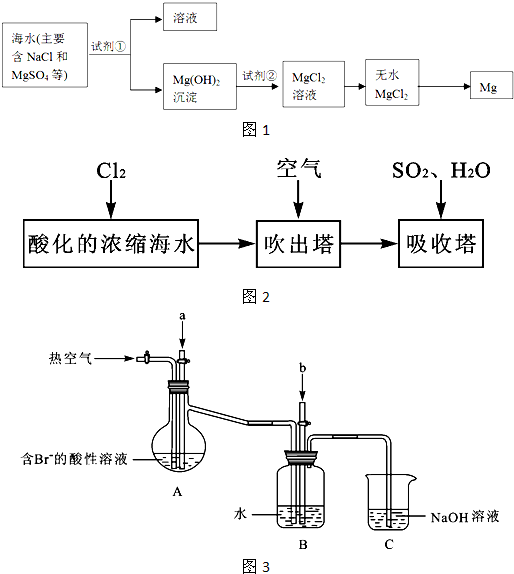
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校研究性学习小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:回答下列问题:

(1)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有 饱和溶液的烧杯中,充分搅拌后经 、 (填操作方法)可得纯净的Mg(OH)2。写出有关反应的离子方程式 。
(2)右图是该校研究性学习小组设计进行过程③的实验装置图。其中装置A的作用是 。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是 。

(3)写出过程④中发生反应的化学方程式 。该过程得到的镁蒸气需要在特定的循环中冷却,应选用 (填试剂名称)作冷却剂。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
| FeBr3 |
| FeBr3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
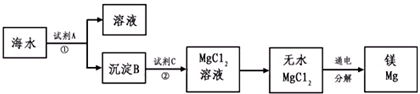
科目:高中化学 来源: 题型:阅读理解
| △ |
| 电解 |
| 2800℃ |
| △ |
| C |
| 还原 |
| HCl |
| ||
| 714℃ |
| HCl |
| 活泼金属 |
| 还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com