
下列溶液中的氯离子数目与50 mL 1 mol/L的AlCl3溶液中氯离子数目相等的是
A.75 mL 2 mol/L的CaCl2 B.150 mL 1 mol/L的NaCl
C.150 mL 3 mol/L的KCl D.100 mL 2 mol/L的NH4Cl
B
【解析】
试题分析:根据物质的化学式及物质的物质的量浓度来计算氯离子的数目,50 mL 1 mol·L-1氯化铝溶液中氯离子的物质的量浓度1mol/L×3=3mol/L,数目为0.15mol,A. 75 mL 2 mol·L-1氯化钙溶液中氯离子的物质的量浓度为2mol/L×2=4mol/L ,数目为0.3mol错误;B. 150 mL 1.0 mol·L-1氯化钠溶液中氯离子浓度为1.0mol/L×1=1mol/L,数目为0.15mol,正确;C、150 mL 3 mol·L-1氯化钾溶液中氯离子浓度为3mol/L×1=3mol/L,数目为0.45mol错误 ;D. 100 mL 2 mol·L-1氯化铵溶液中氯离子浓度为2mol/L×1=2mol/L;数目为0.2mol错误;选B。
考点:考查离子浓度的计算。


科目:高中化学 来源:2014-2015学年广东省东莞市三校高二上学期期中联考化学试卷(解析版) 题型:选择题
大气臭氧层的反应是:O+O3=2O2 ΔH,该反应的能量变化如图所示,下列叙正确的是

A.O+O3=2O2是吸热反应
B.O+O3=2O2是放热反应
C.反应O+O3=2O2的 ΔH=E3-E2
D.反应O+O3=2O2的 ΔH=E3-E1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
某有机物完全燃烧生成CO2和H2O。将12 g该有机物完全燃烧的产物通过浓H2SO4,浓H2SO4增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。则该有机物的分子式为
A.C4H10 B.C2H6O
C.C3H8O D.C2H4O2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
下列有关有机物的说法中正确的是:
A.凡是含碳元素的化合物都属于有机物;
B.易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物;
C.所有的有机物都很容易燃烧;
D.有机物所起的反应,一般比较复杂,速度缓慢,并且还常伴有副反应发生。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省东莞市三校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.氧化剂本身发生氧化反应
B.氧化还原反应一定有氧元素参加
C.氧化剂在反应中得电子,还原剂失去电子
D.氧化反应一定先于还原反应发生
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二上学期第二次月考化学试卷(解析版) 题型:填空题
(12分)工业制氢气的一个重要反应是:CO(g)+H2O(g)  CO2(g)+H2(g)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
CO2(g)+H2(g)现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡状态所需时间/min | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
II | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
①对于反应CO(g)+H2O(g)  CO2(g)+H2(g),下列说法正确的是
CO2(g)+H2(g),下列说法正确的是
A.当容器中CO的含量保持不变时,说明该反应达到平衡状态
B.若混合气体的密度不再改变,说明该反应已达化学平衡状态
C.实验I中,反应达到平衡后,再通入4molCO和2molH2O,平衡正向移动,H2的体积分数增大
D.若使用催化剂,会改变反应的途径,但反应的焓变不变
②实验I中,从反应开始到反应达到平衡时,CO的平均反应速率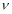 (CO)= ;
(CO)= ;
③实验II条件下反应的平衡常数K= (保留小数点后二位);H2O(g)的平衡转化率为 。
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1.5molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则平衡向 方向移动(填“正反应”、“逆反应”或“不移动”)
⑤若仅改变温度,纵坐标y随T变化如图所示,则纵坐标y表示的是 。
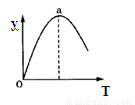
A.CO2的百分含量 B.混合气体的平均相对分子质量
C.CO的转化率 D.H2O的物质的量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高二上学期第二次月考化学试卷(解析版) 题型:选择题
工业废水中常含有Cu2+、Cd2+、Pb2+等重金属离子,可通过加入过量的难溶电解质FeS、MnS,使这些金属离子形成硫化物沉淀除去。根据以上事实,可推知FeS、MnS具有的相关性质是
A.在水中的溶解能力大于 CuS、CdS、PbS
B.在水中的溶解能力小于CuS、CdS、PbS
C.在水中的溶解能力与CuS、CdS、PbS相同
D.二者均具有较强的吸附性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省校高一上学期期中化学试卷(解析版) 题型:选择题
已知0.1mol X2O72- 能将100mL,3mol/L SO32- 氧化成SO42-,则X元素被还原后的化合价是
A.0 B.+2 C.+3 D.+4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高二上学期期中化学试卷(解析版) 题型:填空题
(6分)把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+ O2(g)=====CO2(g);ΔH1<0 ①
途径Ⅱ 先制成水煤气:
C(s)+H2O(g)=====CO(g)+H2(g);ΔH2>0 ②
再燃烧水煤气:
2CO(g)+O2(g)=====2CO2(g);ΔH3<0 ③
2H2(g)+O2(g)=====2H2O(g);ΔH4<0 ④
请回答下列问题:
(1)途径Ⅰ放出的热量_________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com