
| ²½Ö豹ŗÅ | ²Ł×÷¹ż³Ģ | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ¢Ł | ĀČĖ®ÓŠĖįŠŌ | ||
| ¢Ś | ĀČĖ®ÓŠĘư׊Ō | ||
| ¢Ū | ĀČĖ®ÖŠ“ęŌŚCl- |
·ÖĪö ±¾ŹµŃéĪŖĀČĘųµÄŠŌÖŹŹµŃ飬¶¼ŹĒµÄŌŚŹŌ¹ÜÄŚĶź³É£¬ÓƵ½µÄÖ÷ŅŖŅĒĘ÷ĪŖŹŌ¹Ü¼°½ŗĶ·µĪ¹Ü£¬ŅĄ¾ŻŹµŃéÄæµÄŃ”ŌńŠčŅŖµÄŅ©Ę·£¬ŃéÖ¤ĖįŠŌæÉŅŌÓƵĪÓŠ·ÓĢŖµÄĒāŃõ»ÆÄĘČÜŅŗ£¬ŃéÖ¤ĀČĖ®µÄĘư׊Ō£¬æÉŅŌŃ”ŌńĘ·ŗģČÜŅŗ£¬ŃéÖ¤ĀČĄė×Ó£¬Ó¦ĻČ¼ÓĻõĖįÅųżŌÓÖŹĄė×ÓµÄøÉČÅ£¬Č»ŗó¼ÓČėĻõĖįŅų£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ±¾ŹµŃéĪŖĀČĘųµÄŠŌÖŹŹµŃ飬¶¼ŹĒµÄŌŚŹŌ¹ÜÄŚĶź³É£¬ÓƵ½µÄÖ÷ŅŖŅĒĘ÷ĪŖŹŌ¹Ü¼°½ŗĶ·µĪ¹Ü£»
ŅĄ¾ŻŹµŃéÄæµÄŃ”ŌńŠčŅŖµÄŅ©Ę·£¬ŃéÖ¤ĖįŠŌæÉŅŌÓƵĪÓŠ·ÓĢŖµÄĒāŃõ»ÆÄĘČÜŅŗ£¬ŃéÖ¤ĀČĖ®µÄĘư׊Ō£¬æÉŅŌŃ”ŌńĘ·ŗģČÜŅŗ£¬ŃéÖ¤ĀČĄė×Ó£¬Ó¦ĻČ¼ÓĻõĖįÅųżŌÓÖŹĄė×ÓµÄøÉČÅ£¬Č»ŗó¼ÓČėĻõĖįŅų£¬ĖłŅŌÓƵ½µÄŅ©Ę·ÓŠ£ŗĘ·ŗģČÜŅŗ”¢ĻõĖįŅųČÜŅŗ”¢Ļ”ĻõĖį£»
ŃéÖ¤ĖįŠŌæÉŅŌĻņµĪÓŠ·ÓĢŖµÄĒāŃõ»ÆÄĘČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŠĀÖʵı„ŗĶĀČĖ®£¬Č»ŗóÕńµ“£¬ČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ«£¬¼“æÉÖ¤Ć÷ĀČĖ®ÓŠĖįŠŌ£»
ŃéÖ¤ĀČĖ®µÄĘư׊Ō£¬æÉŅŌŃ”ŌńĘ·ŗģČÜŅŗ£¬ĻņŹ¢ÓŠĘ·ŗģČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŠĀÖʵı„ŗĶĀČĖ®£¬ČōČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ«£¬æÉÖ¤Ć÷ĀČĖ®ÓŠĘư׊Ō£»
ŃéÖ¤ĀČĄė×Ó£¬Ó¦Č”ÉŁĮæµÄŠĀÖʱ„ŗĶĀČĖ®ÓŚŹŌ¹Ü ÖŠ£¬µĪČė¼øµĪĻõĖįŅųČÜŅŗ£¬Čō²śÉś°×É«³Įµķ£¬Č»ŗó¼ÓČėĻõĖį£¬°×É«³Įµķ²»ĻūŹ§£¬¼“æÉÖ¤Ć÷ĀČĖ®ÖŠŗ¬ÓŠĀČĄė×Ó£»
Čō²½Öč¢ŁÖŠŹ¹ÓĆĮĖµĪÓŠ·ÓĢŖµÄĒāŃõ»ÆÄĘČÜŅŗ£¬ČÜŅŗŗģÉ«ĶŹÉ«£¬ÓŠĮ½ÖÖæÉÄÜŌŅņ£ŗŅ»ŹĒĀČĖ®ÖŠµÄĖįÖŠŗĶĮĖĒāŃõ»ÆÄĘČÜŅŗ£¬“ĖŹ±·ÓĢŖ²¢Ī“·¢Éśøı䣬¶žŹĒĀČĘųÓėĖ®Éś³ÉµÄ“ĪĀČĖįŃõ»Æ·ÓĢŖĘĘ»µĮĖ·ÓĢŖµÄ½į¹¹¶ųĶŹÉ«£®ĻŌČ»£¬Ö»ŅŖÖ¤Ć÷ČÜŅŗÖŠŹĒ·ńŗ¬ÓŠ·ÓĢŖ£¬¾ĶÄÜČ·¶ØŹĒÄĒÖÖŌŅņ£¬æÉŅŌĻņĶŹÉ«µÄČÜŅŗÖŠŌŁµĪČėŅ»µĪĒāŃõ»ÆÄĘČÜŅŗ£¬ČōÓÖĻŌŗģÉ«ĖµĆ÷ŹĒŅņĪŖÖŠŗĶ¶ųĶŹÉ«£¬ČōĪŽŗģÉ«³öĻÖĖµĆ÷ŹĒŅņŃõ»Æ¶ųĶŹÉ«£»
¹Ź“š°øĪŖ£ŗ
ŹµŃéÓĆĘ·£ŗŹŌ¹Ü”¢½ŗĶ·µĪ¹Ü
Ń”ÓĆŹŌ¼Į£ŗĘ·ŗģČÜŅŗ”¢ĻõĖįŅųČÜŅŗ”¢Ļ”ĻõĖį£»
ŹµŃé¼ĒĀ¼±ķ£ŗ
| ²½Ö豹ŗÅ | ²Ł×÷¹ż³Ģ | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ¢Ł | ȔɣĮæµĪÓŠ·ÓĢŖµÄĒāŃõ»ÆÄĘČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėŠĀÖʵı„ŗĶĀČĖ®£¬Č»ŗóÕńµ“ | ČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ« | ĀČĖ®ÓŠĖįŠŌ |
| ¢Ś | ĻņÉŁĮæŹ¢ÓŠĘ·ŗģČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŠĀÖʵı„ŗĶĀČĖ®£¬Õńµ“ | ČÜŅŗÓÉŗģÉ«±äĪŖĪŽÉ« | ĀČĖ®ÓŠĘư׊Ō |
| ¢Ū | ȔɣĮæµÄŠĀÖʱ„ŗĶĀČĖ®ÓŚŹŌ¹Ü ÖŠ£¬µĪČė¼øµĪĻõĖįŅųČÜŅŗ£¬ŌŁµĪ¼ÓĻ”ĻõĖį | ÓŠ°×É«³Įµķ²śÉś | ĀČĖ®ÖŠ“ęŌŚCl- |
µćĘĄ ±¾Ģāæ¼²éĮĖĀČĖ®ŠŌÖŹĢ½¾æŹµŃéÉč¼Ę£¬Ć÷Č·ŹµŃéÄæµÄ¼°ĀČĘų”¢“ĪĀČĖįŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬×¢ŅāŹµŃéÉč¼ĘµÄŃĻĆÜŠŌ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | S£Øg£©+O2£Øg£©ØTSO2£Øg£©”÷H1£»S£Øs£©+O2£Øg£©ØTSO2£Øg£©”÷H2£¬Ōņ”÷H1£¼”÷H2 | |
| B£® | C£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H=+1.9 kJ•mol-1£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| C£® | NaOH£Øaq£©+HCl£Øaq£©ØTNaCl£Øaq£©+H2O£Øl£©”÷H=-57.4 kJ•mol-1£¬Ōņŗ¬20 g NaOHµÄĻ”ČÜŅŗÓėĻ”“×ĖįĒ”ŗĆĶźČ«·“Ó¦£¬·Å³öµÄČČĮæĪŖ28.7 kJ | |
| D£® | 2C£Øs£©+O2£Øg£©ØT2CO£Øg£©”÷H=-221 kJ•mol-1£¬ŌņĢ¼µÄČ¼ÉÕČȵČÓŚ110.5 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ×°ÖĆ¼×ÖŠĶʬ±ķĆę²śÉśĘųÅŻ | |
| B£® | ×°ÖĆ¼×ČÜŅŗÖŠSO42”„ĻņĶʬ×ö¶ØĻņŅĘ¶Æ | |
| C£® | ×°ÖĆŅŅÖŠµē×Ó“ÓĶʬ¾µ¼ĻßĮ÷ĻņŠæʬ | |
| D£® | ×°ÖĆŅŅÖŠÕż¼«µÄµē¼«·“Ó¦Ź½£ŗ2H++2e”„ØTH2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| Ka1 | Ka2 | |
| H2SO3 | 1.3”Į10-2 | 6.3”Į10-8 |
| H2CO3 | 4.2”Į10-7 | 5.6”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
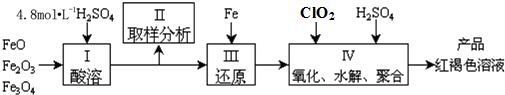
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
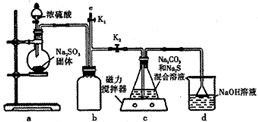 Ģģ½ņøŪ”°8.12”±±¬ÕØŹĀ¹ŹÖŠ£¬Ņņ±¬Õسå»÷µ¼ÖĀĒč»ÆÄĘŠ¹Ā©£¬æÉŅŌĶعżÅēČ÷Ė«ŃõĖ®»ņĮņ“śĮņĖįÄĘČÜŅŗĄ““¦Ąķ£¬ŅŌ¼õĒįĪŪČ¾£®
Ģģ½ņøŪ”°8.12”±±¬ÕØŹĀ¹ŹÖŠ£¬Ņņ±¬Õسå»÷µ¼ÖĀĒč»ÆÄĘŠ¹Ā©£¬æÉŅŌĶعżÅēČ÷Ė«ŃõĖ®»ņĮņ“śĮņĖįÄĘČÜŅŗĄ““¦Ąķ£¬ŅŌ¼õĒįĪŪČ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Al£ØOH£©3 | Fe£ØOH£©2 | Fe£ØOH£©3 | |
| æŖŹ¼³ĮµķŹ± | 3.4 | 6.3 | 1.5 |
| ĶźČ«³ĮµķŹ± | 4.7 | 8.3 | 2.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
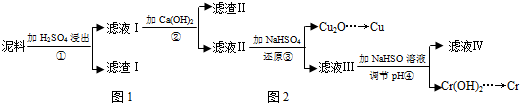
| Fe3+ | Cu2+ | Cr3+ | |
| æŖŹ¼³ĮµķpH | 2.1 | 4.7 | 4.3 |
| ĶźČ«³ĮµķpH | 3.2 | 6.7 | a |
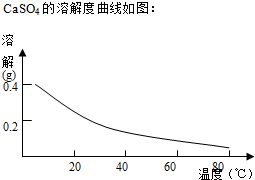
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±„ŗĶĀČĖ®ÖŠ£ŗCl-”¢NO3-”¢Na+”¢SO32- | |
| B£® | $\frac{K_W}{{c£Ø{H^+}£©}}$=10-13mol•L-1ČÜŅŗÖŠ£ŗNH4+”¢Mg2+”¢NO3-”¢SO32- | |
| C£® | ĶØČė“óĮæCO2µÄČÜŅŗÖŠ£ŗNa+”¢SO32-”¢CH3COO-”¢HCO3- | |
| D£® | Na2SČÜŅŗÖŠ£ŗSO42-”¢K+”¢Cl-”¢Cu2+ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com