
【题目】甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景。在催化剂作用下可用H2和CO合成甲醇,反应的化学方程式为 2H2(g)+CO(g)![]() CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图所示。
CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图所示。

回答下列问题:
(1)代表H2浓度变化的曲线为_______(填“a”、“b”或“c”)。
(2)提出一条可以加快反应速率的措施:______________________________。
(3)04 min内,CH3OH的平均反应速率为_________________。
(4)我国某高校化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。

①该电池工作时,c口通入的物质为_____________,该电极为____(填“正极”或“负极”)。
②该电池工作一段时间后,,当6.4 g甲醇完全反应生成CO2时,消耗的氧气的体积为_____L(标准状况下)。
【答案】 a 增大压强(或升高温度等其他合理答案) 0.15 mol L-l min-1 O2(或空气) 正极 6.72
【解析】(1)由2H2(g)+CO(g)![]() CH3OH反应,H2浓度变化在减小并且是CO的2倍,所以代表H2浓度变化的曲线为a,故答案为:a;
CH3OH反应,H2浓度变化在减小并且是CO的2倍,所以代表H2浓度变化的曲线为a,故答案为:a;
(2)可以加快反应速率的措施为加压或者升温,故答案为:加压或者升温;
(3)根据图象CH3OH为生成物,即代表CH3OH浓度变化的曲线为b,则0-4 min内,CH3OH的平均反应速率=![]() =
=![]() =0.15mol/(Lmin),故答案为:0.15mol/(Lmin);
=0.15mol/(Lmin),故答案为:0.15mol/(Lmin);
(4)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以c口通入的物质为氧气,故答案为:O2;正极;
②当6.4g即0.2mol甲醇完全反应生成CO2时,根据总反应:2CH3OH+3O2=2CO2+4H2O,消耗氧气0.3mol,即标准状况下体积为0.3×22.4=6.72L,故答案为:6.72。


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】对下图中两极加以必要的联接并填空:
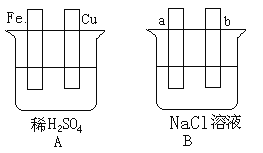
(1)在A图中,请加以必要联接,使铜片上冒H2气泡。________
Fe片的电极反应式:________________,溶液中SO42-向____(填“铁”或“铜”)片迁移。
(2)在B图中,请加以必要联接,使b极析出Cl2。总反应方程式:___________________。
(3)若将A、B串联(a接Cu,b接Fe),则a极析出的物质是____________。若导线中有0.2mol的电子通过, 则Fe片质量减少________, 同时a电极产生的气体在标准状况下的体积为__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是一种重要的药用元素,缺乏碘能导致甲状腺肿大等.为预防碘缺乏病,目前我国的食盐都是“加碘食盐”.“加碘食盐”中加的是含碘元素的物质是碘酸钾(KIO3),KIO3属于( )
A.酸
B.碱
C.盐
D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原子的一种激发态为1s22s12p1,则该元素在周期表中的位置为
A. 第二周期ⅡA族 B. 第二周期ⅢA族
C. 第二周期ⅠA族 D. 第二周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.化学反应中一定伴随能量变化
B.甲烷燃烧是将全部的化学能转化为热能
C.物质所含化学键键能越大,其越稳定
D.大量燃烧煤炭等化石燃料是造成雾霾天气的重要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F可用于制造香精,可利用下列路线合成。

回答下列问题:
(1)![]() 分子中可能共面的原子最多有_____个;
分子中可能共面的原子最多有_____个;
(2)物质A的名称是______;
(3)物质D中含氧官能团的名称是_______;
(4)“反应④”的反应类型是______;
(5)写出“反应⑥”的化学方程式:________;
(6)C有多种同分异构体,与C中所含有的官能团相同的有_____种,其中核磁共振氢谱为四组峰的结构简式为 和_______。
和_______。
(7)参照上述合成路线,以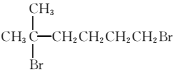 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线:_______________。
的合成路线:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质既可以与盐酸反应,又可以与NaOH溶液反应放出H2,且E的阳离子与A的阴离子核外电子层结构完全相同。

回答下列问题:
(1)A与E形成的化合物的化学式是 __________________。
(2)B的最高价氧化物化学式为_____________,C的元素名称为 __________,D的单质与水反应的方程式为___________________。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是________________________,有关反应的离子方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容积固定的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是

A. 若温度升高,混合气体的颜色变深
B. 在该温度下反应2NO2(g)![]() N2O4(g)的平衡常K为25/9
N2O4(g)的平衡常K为25/9
C. 反应达平衡后,将反应容器的容积减少一半,平衡向正反应方向移动
D. 反应达平衡后,向此容器中通入NO2气体,则c(NO2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B. 25℃时,等体积等物质的量浓度的硝酸与氨水混合后,溶液pH=7
C. 25℃时,0.1mol/L的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D. 25℃时,pH=2的酸HA溶液与pH=12的玻BOH溶液等体积混合后,所得溶液呈酸性,证明HA为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com