
下列与金属腐蚀有关的说法正确的是( )
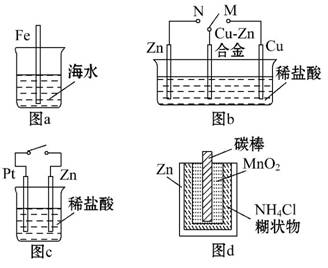
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
下列溶液中能够区别SO2和CO2气体的是 ( )
①澄清石灰水 ②H2S溶液 ③KMnO4酸性溶液 ④氯水 ⑤品红溶液
A.①②③ B.②③④ C.除①以外 D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.NaCl溶液在电流的作用下电离成Na+和Cl-
B.溶于水后能电离出氢离子的化合物都是酸
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钡难溶于水,但硫酸钡属于强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列四种溶液:①1 mol·L-1的盐酸 ②0.1 mol·L-1的盐酸 ③0.01 mol·L-1的NaOH溶液 ④0.001 mol·L-1的NaOH溶液。四种溶液中,由水电离生成的[H+]之比为( )
A.1∶10∶100∶1 000 B.0∶1∶12∶11
C.14∶13∶12∶11 D.14∶13∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
第三代混合动力车,可以用电动机、内燃机或二者结合作为动力。汽车在刹车或下坡时,电池处于充电状态。混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。下图是镍氢电池充放电原理的示意图,其总反应式为H2+2NiOOH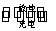 2Ni(OH)2。下列说法中正确的是( )
2Ni(OH)2。下列说法中正确的是( )
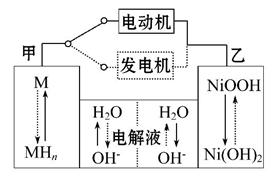
A.混合动力车上坡或加速时,溶液中的OH-向乙电极移动
B.混合动力车刹车或下坡时,乙电极周围溶液的pH增大
C.混合动力车上坡或加速时,乙电极的电极反应式为NiOOH+H2O+e-====
Ni(OH)2+OH-
D.混合动力车刹车或下坡时,甲电极的电极反应式为 H2+2OH-+2e-====2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合成氨工业的叙述,可用勒·夏特列原理来解释的是( )
A.使用铁触媒,使N2和H2混合气体有利于合成氨
B.高压比常压条件更有利于合成氨的反应
C.500℃左右比室温更有利于合成氨的反应
D.合成氨时采用循环操作,可提高原料的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 mL 0.01 mol·L-1 KCl溶液中,加入1 mL 0.01 mol·L-1 AgNO3溶液,下列说法正确的是(AgCl的Ksp=1.8×10-10 mol2·L-2)( )
A.有AgCl沉淀析出 B.无AgCl沉淀
C.无法确定 D.有沉淀但不是AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
向某无色溶液中加入铁粉能产生大量H2,则该溶液中可能含有的能大量共存的离子组是( )
A.Na+、Ca2+、Cl-、NO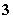
B.Fe3+、K+、Cl-、HCO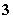
C.Cu2+、Na+、Cl-、SO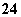
D.K+、Na+、Cl-、SO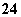
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com