光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性碳催化下合成。
(1)实验室中常用来制备氯气的化学方程式为_________;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为-890.3kJ·mol-1、-285.8 kJ·mol-1和-283.0 kJ·mol-1,则生成1 m3
(标准状况)CO所需热量为___________;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为___________;
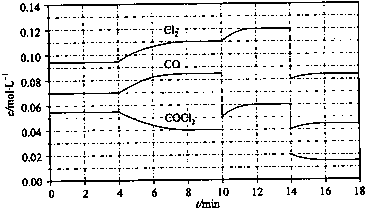
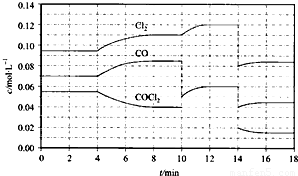
(4)COCl2的分解反应为COCl2(g)= Cl2(g)+ CO(g) △H=+108 kJ·mol-1。反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):
①计算反应在地8min时的平衡常数K=________;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2)___ T(8)(填“<”、“>”或“=” );
③若12min时反应与温度T(8)下重新达到平衡,则此时c(COCl2)=__mol·L-1
④比较产物CO在2-3min、5-6min和12-13min时平均反应速率[平均反应速率分别以v(2-3)、v(5-6)、v(12-13)表示]的大小________;
⑤比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:v(5-6)___ v(15-16)(填“<”、“>”或“=”),原因是_______

 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案