
【题目】1,1-二环丙基乙烯(![]() )是重要医药中间体,下列关于该化合物的说法正确的是
)是重要医药中间体,下列关于该化合物的说法正确的是
A.所有碳原子可能在同一平面B.乙苯与它互为同分异构体
C.二氯代物有9种D.只能发生取代、加成、加聚反应
【答案】C
【解析】
A. 在该物质分子中含有6个饱和碳原子,由于饱和碳原子构成的是四面体结构,所以分子中不可能所有碳原子可能在同一平面,A错误;
B. 乙苯分子式是C8H10,1,1-二环丙基乙烯分子式是C8H12,二者的分子式不相同,因此乙苯与1,1-二环丙基乙烯不是同分异构体,B错误;
C. 该物质分子结构对称,若2个Cl原子在同一个C原子上,有2种不同的结构;若2个Cl原子在不同的C原子上,其中一个Cl原子在不饱和C原子上,可能有2种不同结构;若其中一个Cl原子位于连接在不饱和C原子的环上的C原子上,另一个C原子可能在同一个环上有1种结构;在不同环上,具有2种结构;若一个Cl原子位于-CH2-上,另一个Cl原子在同一个环上,只有1种结构;在两个不同环上,又有1种结构,因此可能的同分异构体种类数目为:2+2+1+2+1+1=9,C正确;
D. 该物质含有不饱和的碳碳双键,可发生加成反应、加聚反应;含有环丙基结构,能够发生取代反应,该物质属于不饱和烃,能够发生燃烧反应,催化氧化反应,因此不仅仅能够发生上述反应,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】利用下列有关装置可进行多种实验,回答下列问题。
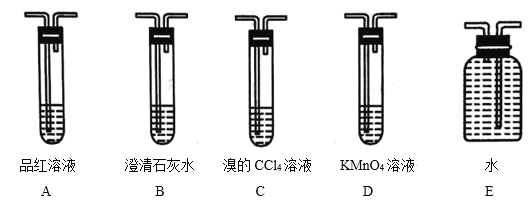
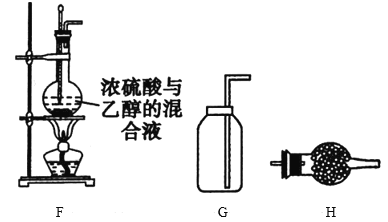
(1)制取并收集一定量的乙烯时必须用到的仪器有___(从题给仪器中选取),写出制备乙烯时的反应方程式:__,实验中,混合浓硫酸与乙醇的方法是__。
(2)已知乙醚的沸点为35℃,利用F装置也可制取乙醚,制备中温度计的水银球位于___(填“溶液中”或“液面上”)。
(3)乙烯制备过程中,烧瓶中的液体很快会变黑,原因是___,生成的气体中除乙烯外还有SO2、CO2气体,为验证上述气体,所用仪器的顺序为FH___,其中H中的试剂是__,确定有乙烯生成的实验现象是__,确定有CO2生成的实验现象是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应
B.C3H6与C4H8一定互为同系物
C.全降解塑料 ![]() 可由环氧丙烷
可由环氧丙烷![]() 和 CO2缩聚制得
和 CO2缩聚制得
D.一定条件下,完全燃烧 14 g 含氧质量分数为 a 的乙烯和乙醛的混合气体,生成水的质量为18(1-a)g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,氯元素的原子核外有____种不同运动状态的电子;有___种不同能级的电子,基态Fe3+的电子排布式为___。
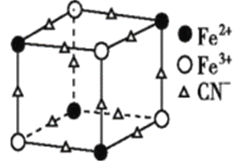
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是____;K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的![]() 结构如图所示(K+未画出),则一个晶胞中的K+个数为 ___。
结构如图所示(K+未画出),则一个晶胞中的K+个数为 ___。
(3)Cu2+能与乙二胺(H2N-CH2-CH2-NH2)形成配离子。该配离子中含有的化学键类型有 __ (填字母)
a.配位键 b.极性键 c.离子键 d.非极性键,

乙二胺中共有____个σ键,C原子的杂化方式为 ___。
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。又知铜的密度为9.0g·cm-3,则铜原子的直径约为____pm。
(5)Cr是周期表中第ⅥB族元素,化合价可以是0~+6的整数价态。回答下列问题。某化合物的化学式为Na3CrO8,其阴离子结构可表示为![]() ,则Cr的化合价为____。CrO42-呈四面体构型,结构为
,则Cr的化合价为____。CrO42-呈四面体构型,结构为![]() ,Cr2O72-由两个CrO42-四面体组成,这两个CrO42-四面体通过共用一个顶角氧原子彼此连接,结构为
,Cr2O72-由两个CrO42-四面体组成,这两个CrO42-四面体通过共用一个顶角氧原子彼此连接,结构为![]() 。则由n(n>1)个CrO42-通过顶角氧原子连续的链式结构的化学式为____。
。则由n(n>1)个CrO42-通过顶角氧原子连续的链式结构的化学式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组在实验室用乙醇、浓硫酸和溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
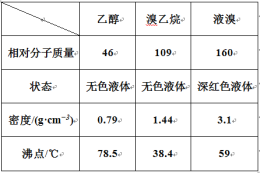
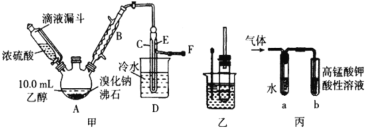
I. 溴乙烷的制备
反应原理如下,实验装置如上图(加热装置、夹持装置均省略):
H2SO4+NaBr ![]() NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr ![]() CH3CH2Br+H2O
CH3CH2Br+H2O
(1) 图甲中A 仪器的名称_____,图中B 冷凝管的作用为_____。
(2) 若图甲中A 加热温度过高或浓硫酸的浓度过大,均会使 C 中收集到的粗产品呈橙色,原因是A 中发生了副反应生成了_____;F 连接导管通入稀NaOH 溶液中,其目的主要是吸收_____等尾气防止污染空气
II. 溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
(3) 在乙中试管内加入 10mL6mol·L -1NaOH 溶液和 2mL 溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4) 若将乙中试管里的 NaOH 溶液换成NaOH 乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a 试管中的水的作用是_______;若无 a 试管,将生成的气体直接通入 b 试管中,则 b中的试剂可以为 _____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应式为C2H5OH+3O2=2CO2+3H2O,电池示意图如下,下列说法中正确的是( )

A.电池工作时,质子向电池的负极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是C2H5OH+3H2O+12e-=2CO2+12H+
D.b极上发生的电极反应是2H2O+O2+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.图1,a点表示的溶液通过升温可以得到b点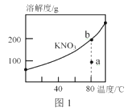
B.图2,若使用催化剂E1、E2、ΔH都会发生改变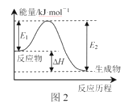
C.图3表示向Na2CO3和NaHCO3的混合溶液中滴加稀盐酸时,产生CO2的情况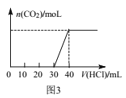
D.图4表示反应aA(g)+bB(g)![]() cC(g),由图可知,a+b>c
cC(g),由图可知,a+b>c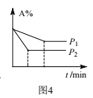
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuCl2溶液。
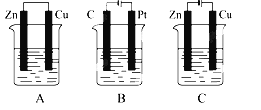
(1)A、B、C三个装置中属于原电池的是________(填标号)。
(2)A池中Zn极发生______反应(填“氧化”或“还原”);Cu是________极,该极的电极反应式为______________________。
(3)B池中Pt是____极,该极的电极反应为________, B池中总反应的化学方程式为________________________________,溶液中阴离子向________(C、Pt)极移动。
(4)C池中Cu极的电极反应为________________,反应过程中,溶液浓度________(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒容密闭容器中充入一定量SO2和O2进行反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0,图甲表示反应速率(v)与温度(T)的关系、图乙表示T1时,平衡体系中SO2的体积分数与压强(p)的关系。下列说法不正确的是( )
2SO3(g)ΔH<0,图甲表示反应速率(v)与温度(T)的关系、图乙表示T1时,平衡体系中SO2的体积分数与压强(p)的关系。下列说法不正确的是( )
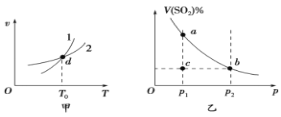
A.图甲中,曲线1表示逆反应速率与温度的关系
B.图甲中,d点时,混合气体的平均摩尔质量不再改变
C.图乙中,a、b两点的反应速率:va>vb
D.图乙中,c点的正、逆反应速率:v(逆)>v(正)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com