
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有20 种元素 | |
| C. | 科学研究时,经常在金属、非金属分界处寻找半导体材料 | |
| D. | 元素周期表共七个横行代表七个周期,18 个纵列代表18 个族 |
分析 A.副族元素、第ⅤⅢ族元素统称为过渡元素;
B.短周期含一、二、三周期;
C.金属与非金属交界处附近的元素具有金属性、非金属性;
D.周期表有7个周期、16个族.
解答 解:A.副族元素、第ⅤⅢ族元素统称为过渡元素,过渡元素包含副族元素,故A错误;
B.短周期含一、二、三周期,则有2+8+8=18种元素,故B错误;
C.金属与非金属交界处附近的元素具有金属性、非金属性,可在金属、非金属分界处寻找半导体材料,故C正确;
D.周期表有7个周期、16个族,8、9、10三个纵行为第ⅤⅢ族,故D错误;
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,把握周期表的结构、元素在周期表的位置为解答的关键,侧重分析与应用能力的考查,注意第ⅤⅢ族及过渡元素的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
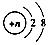 ,下列有关该粒子的说法中不正确的是( )
,下列有关该粒子的说法中不正确的是( )| A. | M粒子的符号可能是O2-、Ne、Mg2+等 | |
| B. | n值只有5种可能 | |
| C. | 取含有M粒子的溶液进行焰色反应,若为黄色,则M的符号是Na+ | |
| D. | n=13时,含M粒子的溶液加入过量的氨水,最终有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲溶液中c(CH3COO-)一定大于乙溶液中c(CH3COO-) | |
| B. | 甲、乙等体积混合后pH大于2 | |
| C. | 乙溶液离子浓度大小关系为:c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 加入相同浓度的NaOH溶液至中性,甲乙两溶液消耗NaOH溶液的体积相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是直线形结构 | |
| B. | 中心原子都采取 sp1杂化 | |
| C. | 硫原子和碳原子上都没有孤对电子 | |
| D. | SO2 为 V 形结构,CO2为直线形结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO4、H2SO4、H3PO4的酸性依次增强 | |
| B. | P、S、F最高正价依次升高 | |
| C. | HCl、HBr、HI的稳定性依次增强 | |
| D. | 锂、钠、钡的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质(杂质) | 除杂质所用试剂及方法 |
| A | 乙醇(水) | 加入生石灰蒸馏 |
| B | 苯(苯酚) | 加入浓溴水振荡后过滤 |
| C | 溴乙烷(溴单质) | 加入NaHSO3溶液振荡、静置、分液 |
| D | 甲烷(乙烯) | 依次通过KMnO4酸性溶液、NaOH溶液洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com