
短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2﹣具有相同的电子层结构,W与X同主族.下列说法正确的是( )
|
| A. | Y的气态简单氢化物的热稳定性比W的强 |
|
| B. | X的最高价氧化物对应水化物的酸性比W的弱 |
|
| C. | Y分别与Z、W形成的化合物均为碱性氧化物 |
|
| D. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| 原子结构与元素周期律的关系.. | |
| 分析: | 短周期主族元素X、Y、Z、W的原子序数依次增大,Y是地壳中含量最高的元素,则Y是O元素,Z2+与Y2﹣具有相同的电子层结构,则Z是Mg元素,W与X同主族,X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个、第一层为最外层不超过2个,X原子序数小于Y,则X是C元素,W是Si元素, A.元素的非金属性越强,其气态氢化物的稳定性越强; B.元素的非金属性越强,其最高价氧化物的水化物酸性越强; C.Y是O元素、Z是Mg元素、W是Si元素,SiO2是酸性氧化物; D.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小. |
| 解答: | 解:短周期主族元素X、Y、Z、W的原子序数依次增大,Y是地壳中含量最高的元素,则Y是O元素,Z2+与Y2﹣具有相同的电子层结构,则Z是Mg元素,W与X同主族,X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个、第一层为最外层不超过2个,X原子序数小于Y,则X是C元素,W是Si元素, A.元素的非金属性越强,其气态氢化物的稳定性越强,Y的非金属性大于W,所以Y的气态简单氢化物的热稳定性比W的强,故A正确; B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性X>W,所以X的最高价氧化物对应水化物的酸性比W的强,故B错误; C.Y是O元素、Z是Mg元素、W是Si元素,SiO2是酸性氧化物,MgO是碱性氧化物,故C错误; D.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径r(Z)>r(W)>r(X)>r(Y),故D错误; 故选A. |
| 点评: | 本题考查原子结构和元素周期律,明确元素周期律内涵是解本题关键,熟练掌握元素周期律并灵活运用,知道非金属的非金属性与其气态氢化物的稳定性、最高价氧化物的水化物酸性强弱关系,题目难度不大. |


科目:高中化学 来源: 题型:
已知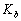 = 1.8 ×10-5,计算 0.10 mol·L-1 的 NH3·H2O 的 ;若向其中加入固体NH4Cl ,使 的浓度达到 0.20 mol·L-1 ,求 。
= 1.8 ×10-5,计算 0.10 mol·L-1 的 NH3·H2O 的 ;若向其中加入固体NH4Cl ,使 的浓度达到 0.20 mol·L-1 ,求 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在制定溶液中一定能大量共存的是 ( )
A.澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl-
B.c(Fe3+)=0.1mol·Lˉ1的溶液中:Na+、NH4+、SCN-、SO42-
C.加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3-
D.0.1mol·Lˉ1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
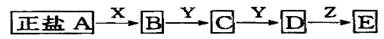 |
当X是强酸时,A、B、C、D、E均含有同一种元素;当X是强碱时,A、B、C、D、E均含有另一种元素
回答下列问题(用化学式填写):
(1)A是________________,Y是_______________,Z是________________.
(2)当X是强碱时,E是________________.
(3)当X是强酸时,E是________________.
(4)写出A与X(是强酸时)反应的离子方程式__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值.下列说法正确的是( )
|
| A. | 1L 1mol•L﹣1的NaClO 溶液中含有ClO﹣的数目为NA |
|
| B. | 标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA |
|
| C. | 铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标况下) |
|
| D. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3,若将X通入澄清石灰水中,无沉淀产生,则有关气体X的成分的下列说法正确的是( )
①一定含有HBr,可能含有CO2 ②一定不含CO2 ③一定不含NH3、Cl2 ④可能含有Cl2、CO2.
|
| A. | 只有① | B. | 只有③ | C. | ①和③ | D. | ②和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是
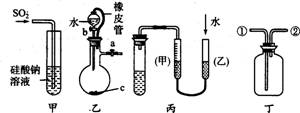
A.甲装置:可用来证明硫的非金属性比硅强
B.乙装置:橡皮管的作用是能使水顺利流下
C.丙装置:用图示的方法能检查此装置的气密性
D.丁装置:可在瓶中先装入某种液体收集NO气体
查看答案和解析>>
科目:高中化学 来源: 题型:
A与B在容积为1 L的密闭容器中发生反应:aA(s)+bB(g) cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
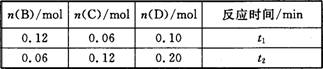
下列说法正确的是
A.0~t1时间段内,平均反应速率v(B)=0.04/t1 mol·(L·min)-1
B.若起始时n(D)=0,则t2时v(D)=0.20/t2 mol·(L·min)-1
C.升高温度,v(B)、vC)、v(D)均增大
D.b:d=6:1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法不正确的是
A.标准状况下C2H4气体22.4L,所含电子数为16NA
B.0.1mol铁在纯氧中充分燃烧,失电子数为0.3NA
C.1L 0.2mol/L的氯化铁溶液中,氯离子数为0.6NA
D.室温下,16g甲烷含有共价键数为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com