
 为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
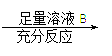 |
方案Ⅱ:铜铝混合物 测定剩余固体的质量
回答下列问题:
⑴小组成员一致认为两个方案都可行,你认为在实验室中选择方案 更便于实施。
⑵小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是 。(填编号)
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
⑶小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45 mL时Al3+开始反应生成成沉淀,当加至溶液的体积为50 mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
【查阅资料】:常温下Ksp[Al(OH)3]=1.0×10-33mol·L-4,Ksp[Cu(OH)2]=2.0×10-20mol·L-3。
①Al(OH)3开始析出时溶液的PH值?
②若溶液中离子的浓度约为1.0×10-5 mol·L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
⑴Ⅱ
⑵AB
⑶①(计算到)c(OH-)=1.0×10-11mol·L-,PH=3
②(计算到)PH=5,Cu(OH)2开始析出
(计算到)PH≈4.7,Al(OH)3沉淀完全
Al(OH)3沉淀完全时,无Cu(OH)2析出。
(1)在中学实验条件下测质量比测气体体积所受的干扰少,精度较高。
(2)易判断,CuSO4溶液与铝会发生置换反应,生成铜单质,这样测出的铜就不是原有的铜了。
(3)根据Ksp[Al(OH)3] = c3(OH-).c(Al3+)即可算出c(OH-)从而算出PH.=3
根据Ksp[Cu(OH)2]=2.0×10-20mol·L-3,c(Cu2+) 已知 ,可算出PH=5时,Cu(OH)2开始析出
根据Ksp[Al(OH)3] = c3(OH-), c(Al3+)=1.0×10-5 mol·L-可算出PH≈4.7,Al(OH)3沉淀完全,所以Al(OH)3沉淀完全时,无Cu(OH)2析出。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
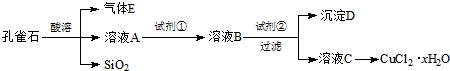
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:
(2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:| 装置 | A (试管+粉末) |
B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
| 高温 |
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
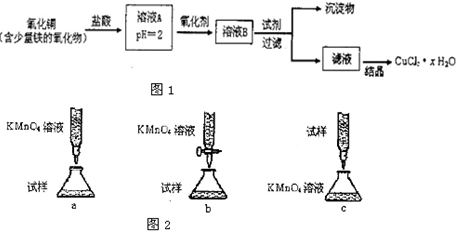
| 80m-135n2 |
| 18n2 |
| 80m-135n2 |
| 18n2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物![]() 测定剩余固体的质量
测定剩余固体的质量
回答下列问题:
(1)小组成员一致认为两个方案都可行,你认为在实验室中选择方案 更便于实施。
(2)小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是 。(填编号)
A.稀盐酸 B.氢氧化钠溶液 C.硫酸铜溶液
(3)小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3?H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45 mL时Al3+开始反应生成沉淀,当加至溶液的体积为50 mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
[查阅资料]:常温下Ksp[Al(OH)3]=1.0×10-33mol?L-4,
Ksp[Cu(OH)2]=2.0×10-20mol?L-3。
请回答下列问题:
①Al(OH)3开始析出时溶液的PH应大于 。
②若溶液中离子的浓度约为1.0×10-5 mol?L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com