
【题目】氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有种,这些电子的电子云形状有种;氟原子的外围电子排布式为 .
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2中所含作用力的类型有;与HF2﹣互为等电子体的分子有(举一例).
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为 , 画出N2F2可能的结构式 .
(4)三氟化硼乙醚(如图1)的熔点为﹣58℃,沸点为126~129℃,它属于晶体.
(5)氟化钙的晶胞结构如图2所示,晶胞参数α=0.555pm. ①Ca2+、F﹣的配位数分别为和 .
②列式表示氟化钙晶体的密度:gcm﹣3(不必计算出结果).
【答案】
(1)9;2;2s22p5
(2)离子键、共价键、氢键;CO2(或Na2O)
(3)sp2;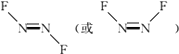
(4)分子
(5)8;4;ρ= ![]()
【解析】解:(1)基态氟原子核外含有9个电子,则其核外电子的运动状态有9种;氟原子核外含有2s轨道和p轨道两种轨道,则氟原子的电子的电子云形状有2种;氟原子的外围含有7个电子,其外围电子排布式为:2s22p5 , 所以答案是:9;2;2s22p5;(2)NaHF2为离子化合物,存在离子键,H﹣F键为共价键,F的电负性较强,还存在氢键,
所以答案是:离子键、共价键、氢键;CO2(或Na2O);(3)N2F2(二氟氮烯)分子中,氮原子形成了3个σ键和1个π键,则其杂化轨道类型为sp2;N2F2可能的结构式为: 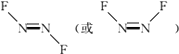 ,
,
所以答案是:sp2; 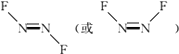 ;(4)三氟化硼乙醚(如图1)的熔点为﹣58℃,沸点为126~129℃,其熔沸点降低,应该属于分子晶体,
;(4)三氟化硼乙醚(如图1)的熔点为﹣58℃,沸点为126~129℃,其熔沸点降低,应该属于分子晶体,
所以答案是:分子;(5)①在CaF2晶胞中每个Ca2+连接4个氟离子,但在下面一个晶胞中又连接4个氟离子,所以其配位数为8;在CaF2晶胞中每个F﹣连接4个钙离子,所以其配位数为4,
所以答案是:8;4;
②该晶胞中含有钙离子个数=8× ![]() +6×
+6× ![]() =4,氟离子在该晶胞的内部,所以氟离子个数是8,该晶胞中含有4个CaF2 , 该晶胞的体积为:V=(5.55×10﹣6)3cm3 , 该晶胞的密度为:ρ=
=4,氟离子在该晶胞的内部,所以氟离子个数是8,该晶胞中含有4个CaF2 , 该晶胞的体积为:V=(5.55×10﹣6)3cm3 , 该晶胞的密度为:ρ= ![]() =
= ![]() ,
,
所以答案是:ρ= ![]() .
.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】下列有关环境保护的叙述中,错误的是
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.工业大量排放二氧化氮是全球气候变暖的主要原因
C.某些装修材料中含有的甲醛、苯等会严重影响人体健康
D.废旧电池中含有的汞、铅、镉等重金属盐对土壤和水源会造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列反应:
①、2H2O+Cl2+SO2=H2SO4+2HCl
②、 KMnO4+ HCl(浓)= KCl+__MnCl2+___Cl2↑+___H2O
针对上述两个反应回答:
(1)配平②的化学方程式________;
(2)用单线桥标出①中电子转移的方向和数目________;
(3)Cl2、SO2和KMnO4的氧化性强弱顺序为____;
(4)反应①中氧化产物和还原产物的物质的量之比为___;
(5)反应②中氯化氢表现出的性质是___。
A.还原性 B.酸性 C.氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.将煤加强热使它分解的过程叫干馏
B.煤经过干馏, 可生产出焦炭、煤焦油、焦炉气等
C.石油经过减压蒸馏, 可以得到更多的汽油
D.石油通过裂化, 可以获得汽油、煤油、润滑油、凡士林和石蜡等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有________性。
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)工业上用洗净的废铜屑作原料来制备硫酸铜。下列制备方法符合“绿色化学”思想的是_______(填序号)。
①Cu+H2SO4(浓)→CuSO4 ②Cu![]() CuO
CuO![]() CuSO4
CuSO4
写出①中反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.
(1)有关热化学方程式如下: 水煤气法:CH4(g)+ ![]() O2(g)═CO(g)+2H2O(g)△H1=﹣35.4KJmol﹣1
O2(g)═CO(g)+2H2O(g)△H1=﹣35.4KJmol﹣1
CO(g)+2H2(g)CH3OH(g)△H2=﹣90.1KJmol﹣1
直接氧化法:
2CH4(g)+O2(g)2CH3OH(g)△H3=KJmol﹣1 .
(2)工业废气二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H.在密闭容器中投入1molCO2和2.75molH2 , 在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示. ①二氧化碳合成甲醇正反应的△H(填“>”“<”或“=”,下同)0.
②M、N两点时化学反应速率:v(M)v(N).
③为提高CO2的转化率除可改变温度和压强外,还可采取的措施是 .
④图中M点时,容器体积为10L,则N点对应的平衡常数K=(填数值,保留2位小数).
(3)一定条件下,向容积不变的某密闭容器中加入amolCO2和bmolH2发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的关系是 . 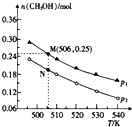
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧和过氧乙酸都是重要的消毒剂。O3可以看成是一个O2携带一个O原子,利用其自身的强氧化性杀死病毒.并放出无污染的O2。下列关于O3的说法中错误的是( )
A.O3与O2互为同素异形体B.O3遇氟氯烃(如CCl2F2)可分解
C.O3使用时浓度大小对人体无害D.O3是一种广谱消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式,不正确的是( )
A.KOH═K++OH﹣
B.NaHCO3Na++HCO3﹣
C.NH3H2ONH4++OH﹣
D.CH3COOHCH3COO﹣+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有100mL含Cu2+、Al3+、NH4+、H+、Cl-的溶液,向该溶液中逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示:
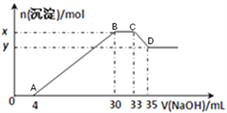
(1)B点的沉淀物的化学式为______________。
(2)原溶液中Cu2+的物质的量为______,原溶液中Cl-物质的量浓度为__________。
(3)原溶液的pH=__________,x-y= _________。
(4)经过滤得到D点的沉淀物,并多次用蒸馏水洗涤沉淀,判断沉淀是否洗涤干净的方法是_________________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com