
| A. | 淡化海水,可向海水中加入净水剂明矾或Na2FeO4 | |
| B. | 金属钠着火,可用水扑灭 | |
| C. | 在电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 | |
| D. | 光导纤维属于有机合成新材料 |
分析 A.明矾或Na2FeO4为净水剂,吸附水中的杂质,与淡化海水无关;
B.钠性质很活泼,易和氧气反应,生成的产物与水、二氧化碳反应生成助燃性的气体氧气;
C.N2与O2在放电的作用下反应生成NO,NO为氧化生成二氧化氮,进而与水反应生成硝酸,最终可生成硝酸盐被农作物吸收;
D.光导纤维的主要成分为二氧化硅.
解答 解:A.淡化海水的方法有多种,如:蒸馏法、结晶法、淡化膜法、多级闪急蒸馏法等,净水剂明矾或Na2FeO4溶于水生成的胶状物对悬浮物进行吸附,使杂质沉降,与海水淡化无关,故A错误;
B.钠燃烧生成过氧化钠,过氧化钠和水、二氧化碳反应生成氧气,促进钠燃烧,故B错误;
C.空气中的N2在放电条件下与O2直接化合生成无色且不溶于水的一氧化氮气体,N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;一氧化氮易与空气中的O2反应生成红棕色的二氧化氮气体,2NO+O2=2NO2;
二氧化氮与水反应生成硝酸(HN03)和一氧化氮,3NO2+H2O=2HNO3+NO,生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好,故C正确;
D.光导纤维的主要成分为二氧化硅,不属于有机合成新材料,故D错误;
故选C.
点评 本题考查较为综合,涉及海水的淡化、钠的性质、氮的固定以及合成材料等知识,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 液态HCl不导电,所以HCl不是电解质 | |
| B. | BaSO4在水中难导电,但熔融状态下能导电,所以BaSO4是电解质 | |
| C. | SO2溶于水能导电,所以SO2是电解质 | |
| D. | NH3溶于水形成的溶液能导电,所以NH3是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


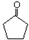 ,G中官能团的名称为碳碳双键、酯基.
,G中官能团的名称为碳碳双键、酯基. ,反应类型加成反应.
,反应类型加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 病人输液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
病人输液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①⑥ | C. | ①④⑤ | D. | 只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 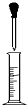 用量筒量取一定量液体时,先从试剂瓶中直接倒入大部分试剂于量筒中,至接近刻度时改用如图所示操作,逐滴加入至刻度 用量筒量取一定量液体时,先从试剂瓶中直接倒入大部分试剂于量筒中,至接近刻度时改用如图所示操作,逐滴加入至刻度 | |
| B. | 金属镁因保存不当造成失火可用细沙盖灭,不能用泡沫灭火器 | |
| C. | 探究温度对化学反应速率影响时,先将硫代硫酸钠与硫酸两种溶液混合后再用水浴加热 | |
| D. | 热化学方程式中,如果没有注明温度和压强,表示反应热是在25℃,101KPa测得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ②③ | C. | ③④⑥ | D. | ②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
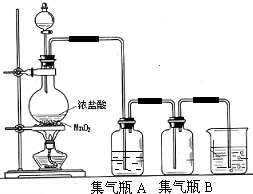
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则H2燃烧热为241.8 kJ•mol-1 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 由BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2kJ•mol-1①BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1②可得反应C(s)+CO2(g)═2CO(g) 的△H=+172.5kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com