
1 L Na2SO4溶液中含Na+ 4.6 g,则溶液中SO 浓度为( )
浓度为( )
A.0.1 mol·L-1 B.0.2 mol·L-1
C.0.6 mol·L-1 D.0.4 mol·L-1
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
常温下,0.1mol·L—1某一元酸(HA)溶液中c(OH—)/c(H+)=1×10—8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10—10mol·L—1
B.溶液中c(H+)+c(A—)=0.1mol·L—1
C.与0.05mol·L—1 NaOH溶液等体积混合所得溶液中离子浓度大小关系为:
c(A—)> c(Na+)> c(OH—)> c(H+)
D.原溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH—)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
将不同量的H2O(气) 和CO 气体分别通入到一体积为l L的恒容密闭容器中进行反应:
H2O (g) + CO( g)  CO2 (g) +H2(g);得到以下三组数据,据此回答下列问题:
CO2 (g) +H2(g);得到以下三组数据,据此回答下列问题:
| 实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
| H2O | CO | H2 | CO | |||
| 1 | 650℃ | 1 mol | 2 mol | 0.8 mol | 1.2 mol | 5 min |
| 2 | 900℃ | 0.5 mol | 1 mol | 0.2 mol | 0.8 mol | 3 min |
| 3 | 900℃ | a | b | c | d | t |
(1)①由以上数据,实验1中以v( CO2) 表示的反应速率为__________。
②该反应在650℃时平衡常数数值为__________,该反应的逆反应为__________ (填“吸” 或“放”)热反应。
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),
且t <3min,则a、b 应满足的关系是__________。
(2)下图1、2 表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
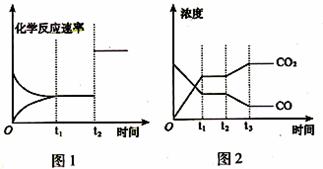 ①图1中时刻t2发生改变的条件可能是__________ (写2条)
①图1中时刻t2发生改变的条件可能是__________ (写2条)
②图2中时刻t2发生改变的条件可能是__________ (写2条)
(3)在850℃时,其平衡常数K = 1,850℃时在该容器中同时充人1.0moICO,3.0 molH2O,1.0molCO2,5.0molH2,此时反应向__________(填“正反应” 或“逆反应”)方向进行,平衡时CO2的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某双原子分子构成的气体,其摩尔质量为M g·mol-1,该气体的质量为m g,阿伏加德罗常数为NA mol-1,则;
(1)该气体在标准状况下的体积为________L;
(2)该气体在标准状况下的密度为________g·L-1;
(3)该气体所含的原子总数为________个;
(4)该气体的一个分子的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.1 mol·L-1的Na2CO3溶液500 mL。
(1)应称取碳酸钠晶体________g。
(2)若称量时砝码与晶体位置左右颠倒,则平衡后实际称得的样品质量为________g(5 g以下使用游码)。
(3)配制溶液时需要用到的仪器有____________________________________。
(4)假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是________。
A.容量瓶洗净后内壁上带有少量蒸馏水
B.定容时,俯视观察刻度线
C.移液时,用于溶解碳酸钠晶体的烧杯没有冲洗
D.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
( )
A.3Br2+6KOH====5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com