
【题目】X,Y,Z三种短周期元素,它们的原子序数之和等于16,X2,Y2,Z2在常温下都是无色气体,它们均为工业合成某化工产品的重要原料,其流程如下:
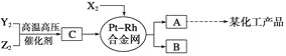
已知:①一定条件下,X2与Y2能反应生成A,X2与Z2能反应生成B;
②B和C分子均为常见的10电子微粒。
请回答下列问题:
(1)X元素在周期表中的位置是___________________________________________;
(2)X2与Z2可制成新型化学电源(KOH溶液作电解质溶液),两个电极均由多孔石墨制成,通入的气体在电极表面放电,负极电极反应式为________________________;
(3)化合物B吸收C后形成的溶液pH______7(填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)___________________________________________________________________;
(4)写出由C生成A和B的化学方程式______________________________。
【答案】第2周期第ⅥA族H2+2OH--2e-=2H2O大于NH3·H2O![]() NH
NH![]() +OH-(或NH3+H2O
+OH-(或NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-)4NH3+5O2
+OH-)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】
![]() ,C分子为常见的10电子微粒,符合
,C分子为常见的10电子微粒,符合![]() ;C是
;C是![]() ,X,Y,Z三种短周期元素,它们的原子序数之和等于16,所以X是O元素;氨气与氧气反应生成NO和
,X,Y,Z三种短周期元素,它们的原子序数之和等于16,所以X是O元素;氨气与氧气反应生成NO和![]() , B为常见的10电子微粒,B是
, B为常见的10电子微粒,B是![]() 、A是NO;O2与Y2能反应生成NO,O2与Z2能反应生成
、A是NO;O2与Y2能反应生成NO,O2与Z2能反应生成![]() ,Z是H元素、Y是N元素。(1)O是8号元素,有2个电子层,最外层6个电子;
,Z是H元素、Y是N元素。(1)O是8号元素,有2个电子层,最外层6个电子;
(2)氢氧燃料电池,负极是氢气失电子发生氧化反应;
(3)水吸收氨气后形成的溶液是氨水,氨水中存在NH3·H2O![]() NH
NH![]() +OH-电离平衡;
+OH-电离平衡;
(4)氨气催化氧化为NO和![]() ;
;
根据以上分析,(1)O是8号元素,有2个电子层,最外层6个电子,所以O元素在周期表中的位置是第2周期第ⅥA族;(2)氢氧燃料电池,负极是氢气失电子发生氧化反应,若以KOH溶液作电解质溶液,负极反应式是H2+2OH--2e-=2H2O;(3)水吸收氨气后形成的溶液是氨水,氨水中存在NH3·H2O![]() NH
NH![]() +OH-电离平衡,所以溶液呈碱性,PH>7;(4)氨气催化氧化为NO和
+OH-电离平衡,所以溶液呈碱性,PH>7;(4)氨气催化氧化为NO和![]() ,反应方程式是4NH3+5O2
,反应方程式是4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;


科目:高中化学 来源: 题型:
【题目】下列仪器用酒精灯加热时,需垫石棉网的是( )
①烧杯 ②坩埚 ③锥形瓶 ④蒸发皿 ⑤试管 ⑥烧瓶 ⑦表面皿
A.②④⑤B.①⑥⑦C.③④⑥D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Fe3O4呈黑色,因其有磁性且粒度小而在磁记录材料、生物功能材料等诸多领域有重要应用,探究其制备和用途意义重大。
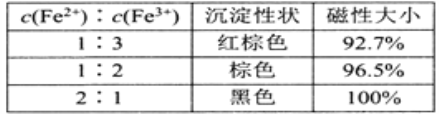
(1)还原-沉淀法:①用还原剂Na2SO3将一定量Fe3+可溶盐溶液中的![]() Fe3+还原,使Fe2+和Fe3+的物质的量比为1:2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:_______。当还原后溶液中c(Fe2+):c(Fe3+)=2:1时,由下表数据可知,产品磁性最大,可能的原因是________________。
Fe3+还原,使Fe2+和Fe3+的物质的量比为1:2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:_______。当还原后溶液中c(Fe2+):c(Fe3+)=2:1时,由下表数据可知,产品磁性最大,可能的原因是________________。
(2)电化学法也可制备纳米级Fe3O4,用面积为4cm2的不锈钢小球(不含镍、铬)为工作电极,铂丝作阴极,用Na2SO4溶液作为电解液,电解液的pH维持在10左右,电流50mA。生成Fe3O4的电极反应为__________。
(3)已知:H2O(1)=H2(g)+![]() O2(g)△H=+285.5kJ·mol-1,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程I的热化学方程式。
O2(g)△H=+285.5kJ·mol-1,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程I的热化学方程式。
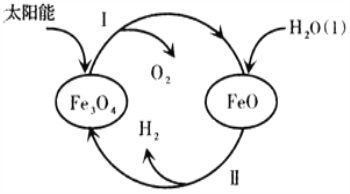
过程I.____________________________________________________。
过程II:3FeO(s)+H2O(1)===H2(g)+Fe3O4(s) △H=+128.9kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O===![]() +2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有关说法正确的是
+2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有关说法正确的是
A. 还原性Cr3+>Fe2+>SO2
B. 氧化性Cr2O72->SO2>Fe3+
C. 两个反应中Fe2(SO4)3均作还原剂
D. Cr2O72-能将Na2SO3氧化成Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2可用作漂白剂和呼吸面具中的供氧剂
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①写出Na2O2作供氧剂的化学反应方程式____________;
②使酚酞溶液变红是因为________,红色褪去的可能原因是___________;
③加入MnO2反应的化学方程式为____________;
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行加下实验,实验步骤和现象如下:
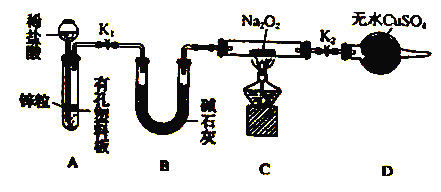
步骤1:按上图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后没有任何现象。
步骤3: ,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是______,B装置的作用_________。
②步骤3在点燃C处酒精灯前必须进行的操作是______________;
③装置D的目的是_________;
④你得到的结论是________(若能反应请用化学方程式表示);
⑤该实验设计中存在着明显不足之处,应该如何改进:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在新制氯水中存在多种分子和离子,下列实验现象和结论一致且正确的是( )
A. 新制氯水使红玫瑰变为白玫瑰,说明有Cl2
B. 加入石蕊溶液,溶液变红,说明该溶液一定不含HClO
C. 将KHCO3固体加入新制的氯水中,有气泡产生,说明有HClO
D. 光照新制氯水有气泡逸出,该气体一定是O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
![]()
(1)写出A、B、C三元素名称________、________、________。
(2)C在元素周期表中的位置是____________________。
(3)B的原子结构示意图为________________,C的氢化物与B的氢化物的稳定性强弱顺序为________>________(填化学式)。
(4)比较A、C的原子半径A________C,写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中,正确的是
A. 一定有氧元素参加 B. 氧化反应一定先于还原反应发生
C. 氧化剂本身发生氧化反应 D. 一定有电子转移(得失或偏向)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 32 g O2占的体积约为22.4 L
B. 1mol N2 含阿伏加德罗常数个氮原子
C. 在标准状况下,22.4 L H2O 的质量约为 18 g
D. 22 g CO2 与标准状况下11.2 L HCl 含有相同分子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com