
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
分析 加入过量的氢氧化钠溶液并加热,铵根离子与氢氧化钠反应生成氨气、亚铁离子与氢氧化钠生成氢氧化铁,再加入足量盐酸后,铵根离子和亚铁离子大量减少;而铜离子和铝离子在反应前后离子的物质的量基本不变,以此解答该题.
解答 解:①加入氢氧化钠溶液生成氢氧化铜,微热后没有变化,再加入盐酸,氢氧化铜与氯化氢反应生成氯化铜和水,反应前后铜离子的物质的量基本不变;
②加入氢氧化钠溶液后生成一水合氨,加热后生成氨气,再加入过量盐酸后,铵根离子大量减少;
③亚铁离子与氢氧化钠溶液反应生成氢氧化亚铁,加热后氢氧化亚铁转化成氢氧化铁,再加入盐酸,氢氧化铁溶解生成铁离子,反应前后亚铁离子大量减少;
④铝离子与过量氢氧化钠溶液反应生成偏铝酸钠,微热后基本无变化,再加入过量盐酸,偏铝酸钠转化成铝离子,反应前后铝离子的物质的量基本不变.
溶液中大量减少的阳离子是②③,
故选B.
点评 本题考查了离子共存、离子反应等知识,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意掌握离子反应发生条件,明确离子共存的判断方法,正确理解题干信息为解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 4:3:3 | C. | 8:6:9 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “Cu-Zn-硫酸”原电池中,电子从Zn经过导线到达Cu,再经过溶液回到Zn形成闭合回路 | |
| B. | “Al-Mg-NaOH”原电池中,活泼型强的Mg失去电子,被氧化,做负极 | |
| C. | 理论上所有自发进行的氧化还原反应均可设计成原电池 | |
| D. | 已知铅蓄电池总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,可推负极是反应是 Pb-2e-=Pb2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
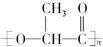 ,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )| A. | 降解塑料是一种纯净物 | |
| B. | 其生产过程中的聚合方式与聚苯乙烯相似 | |
| C. | 它属于一种线型高分子材料 | |
| D. | 其相对分子质量为72 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1000ωνρ}{36.5}$mol/L | B. | $\frac{1000νρ}{36.5+22400}$mol/L | ||
| C. | $\frac{ων}{22.4(V+1)}$mol/L | D. | $\frac{1000νρ}{36.5V+22400}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
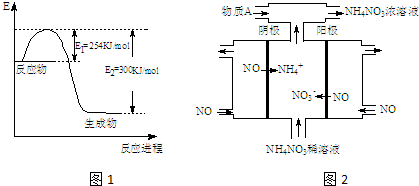
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋白溶胶中加入饱和硫酸铵溶液后有蛋白质析出 | |
| B. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| C. | 因为液态氟化氢中存在氢键,所以其分子比氯化氢更稳定 | |
| D. | 电泳现象可证明胶体属于电解质溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com