
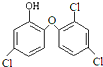
| A、三氯生的分子式是C12H7Cl3O2 |
| B、三氯甲烷与甲烷均无同分异构体 |
| C、1 mol三氯生最多能与6 mol H2反应 |
| D、1 mol三氯生最多能与4mol NaOH反应 |


科目:高中化学 来源: 题型:
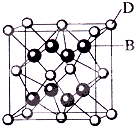 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的 原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如图.
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的 原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如图.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n=m+17Vc | ||||
B、c=
| ||||
C、p=m+
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属元素组成的化合物中只可能含有共价键 |
| B、ⅦA族元素气态氢化物的热稳定性和还原性从上到下依次减弱 |
| C、第三周期非金属元素最高价含氧酸的酸性从左到右依次增强 |
| D、元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com