
【题目】用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液过程中的pH变化如图所示。下列说法错误的是
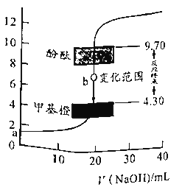
A.b点时,加入极少量NaOH溶液都会引起pH的突变
B.选指示剂时,其变色范围应在4.30~9.70之间
C.若将HCl换成同浓度的CH3COOH,曲线ab段将会上移
D.都使用酚酞做指示剂,若将NaOH换成同浓度的氨水,所消耗氨水的体积较NaOH小
【答案】D
【解析】
A项、b点时,20.00 mL 0.1000 mol/L NaOH溶液与20.00 mL 0.1000 mol/L HCl溶液恰好完全反应,溶液呈中性,若加入极少量NaOH溶液,溶液会变为呈碱性,引起pH的突变,故A正确;
B项、由图可知,滴定时,pH的突跃范围为4.30~9.70,则选指示剂时,指示剂的变色范围应在4.30~9.70之间,故B正确;
C项、若将HCl换成同浓度的CH3COOH,pH的突跃范围会变窄,曲线ab段将会上移,故C正确;
D项、都使用酚酞做指示剂,若将NaOH换成同浓度的氨水,溶液由无色变为浅红色时,得到的是氯化铵和氨水的混合液,氨水过量,消耗氨水的体积较NaOH大,故D错误;
故选D。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)具有优良的杀菌效果,是一种理想的含氯杀菌剂替代品。以低碳钢板作为阳极电解浓氢氧化钠可以迅速制得高铁酸钠,其工作原理如图所示。下列说法正确的是
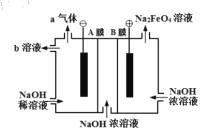
A.“A膜”、“B膜”分别为阴、阳离子交换膜
B.阴极区溶液的pH将减小
C.a气体为H2,,b溶液可循环使用
D.阳极反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)20℃时,在烧杯中加入0.1mol/L的Na2CO3溶液,滴入酚酞呈红色。
①该溶液呈______性(填“酸”“碱”或“中”) ;
②溶液中c( Na+) ____2c(CO32-)(填“>”“<”或“=”);
③滴入酚酞呈红色的原因是___________(用离子力程式表示 )。
(2)工业上常用天然气作为制备CH3OH 的原料。已知:
CH4(g)+O2(g)=CO(g) + H2(g) +H2O(g) △H= -321.5 kJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g) △H= +250.3 kJ/mol
CO(g) +2H2(g)=CH3OH(g) △H= -90.0kJ/mol
则CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为_________。
(3)一定温度和压强下,将2 molSO2和1mol O2置于密闭容器中发生反应2 SO2 (g)+O2(g) ![]() 2SO3(g),并达到平衡。
2SO3(g),并达到平衡。
①若升高温度,SO2的含量增大,则正反应为______ (填“放热”或“吸热”) 反应;
②若再加入1mol O2则SO2的转化率______(填“增大”或“减小”);
③若只增大压强,该反应的化学平衡常数______(填“增大”“减小”或“不变”。
(4)铅蓄电池是化学电源,其电极材料分别起Pb和PbO2,电解质溶液为稀硫酸,工作(放电)时该电池的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。试根据上述情况判断
①铅蓄电池的负极材料是_____ (填“Pb”或“PbO2”) ;
②工作时,电解质溶液的pH_____ (填“ 增大“减小”或“不变” );
③工作时,电解质溶液中阴离子移向_____极 (填“ 负”或“正” )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的绝热密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。下列不能说明该反应达到化学平衡状态的是
2NH3(g) △H<0。下列不能说明该反应达到化学平衡状态的是
A.混合气体的密度不变B.体系温度不变
C.3v逆(NH3)=2v正(H2)D.N2和NH3的浓度的比值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
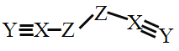
A.化合物WY是良好的耐热冲击材料
B.Y的氧化物对应的水化物可能是弱酸
C.X的氢化物的沸点一定小于Z的
D.化合物(ZXY)2中所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶洞的形成主要源于石灰岩受地下水的长期溶蚀,发生反应:CaCO3+CO2+H2O=Ca(HCO3)2。当受热或压强突然减小时溶解的Ca(HCO3)2会分解,从而形成钟乳石、石笋等奇妙景观。
(1)写出Ca(HCO3)2受热分解的离子方程式____;从平衡移动的角度解释压强减小时Ca(HCO3)2分解的原因_______。
(2)向Ca(HCO3)2饱和溶液中滴加酚酞,溶液呈很浅的红色。由此可得到的结论是:饱和溶液中Ca(HCO3)2水解程度__________且___________。
(3)常温下,H2CO3的电离常数Ka2=4.7×10-11。若测得5.0×10-3 mol/L Ca(HCO3)2溶液的pH为8.0,则溶液中c(CO32-)与c(OH-)的比值为___________(简要写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中含有大量氮氧化物NOx,工业脱硝技术成为研究热点。
(1)汽车尾气中NO和CO可利用车载催化剂转化为无毒物质排放。
已知:N2(g)+O2(g)=2NO(g) △H1=+183 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-565 kJ·mol-1
写出催化转化的热化学方程式_________。
(2)臭氧氧化-碱吸收法可有效脱除NO,氧化原理为:NO(g)+O3(g)![]() NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
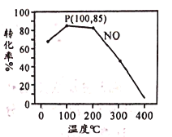
①100℃时,从开始反应到P点的平均反应速率v(NO)=__________。
②反应时同时发生副反应:2O3![]() 3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为________mol。
3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为________mol。
(3)选择性催化还原技术(NCR)可在较低温度下脱硝,原理如图I,天然锰矿可作催化剂。
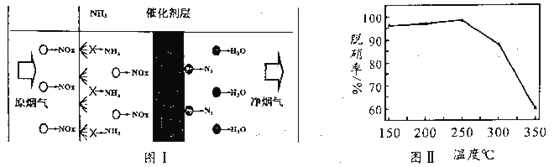
以NO代表氮氧化物,写出反应方程式_____________________;实验测得脱硝率随温度的变化如图II所示,请分析温度高于250℃时脱硝率下降的原因可能是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值。下列有关叙述正确的是
A.在 12.0g NaHSO4 晶体中,所含离子数目为 0.3NA
B.足量的镁与浓硫酸充分反应,放出 2.24L 混合气体时,转移电子数为 0.2NA
C.30g 冰醋酸和葡萄糖的混合物中含氢原子的数目为 2NA
D.标准状况下,11.2L 乙烯和丙烯混合物中含氢原子数目为 2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国格勒诺布尔(Grenoble)约瑟夫·傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶的作用下发生反应:C6H12O6+6O2![]() 6CO2+6H2O(酸性环境)。下列有关该电池的说法不正确的是( )
6CO2+6H2O(酸性环境)。下列有关该电池的说法不正确的是( )
A. 该生物燃料电池不可以在高温下工作
B. 电池的负极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+
C. 消耗1 mol氧气时转移4 mol e-,H+向负极移动
D. 今后的研究方向是设法提高葡萄糖生物燃料电池的效率,从而使其在将来可以为任何可植入医疗设备提供电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com