
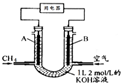
 ½«CH4Éč¼Ę³ÉČ¼ĮĻµē³Ų£¬ĘäĄūÓĆĀŹøüøߣ¬×°ÖĆČēĶ¼ĖłŹ¾£ØA”¢BĪŖ¶ąæ׊ŌĢ¼°ō£©³ÖŠųĶØČė¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéĢå»żVL£®Ķź³ÉĻĀĮŠĪŹĢā£ŗ
½«CH4Éč¼Ę³ÉČ¼ĮĻµē³Ų£¬ĘäĄūÓĆĀŹøüøߣ¬×°ÖĆČēĶ¼ĖłŹ¾£ØA”¢BĪŖ¶ąæ׊ŌĢ¼°ō£©³ÖŠųĶØČė¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéĢå»żVL£®Ķź³ÉĻĀĮŠĪŹĢā£ŗ·ÖĪö Č¼ĮĻµē³ŲÖŠ£¬ĶØČėČ¼ĮĻµÄŅ»¶ĖĪŖŌµē³ŲµÄøŗ¼«£¬ĶØČėæÕĘųµÄŅ»¶ĖĪŖŌµē³ŲµÄÕż¼«£¬ŅõĄė×ÓĻņøŗ¼«ŅĘ¶Æ£¬ŃōĄė×ÓŅĘĻņÕż¼«£¬n£ØKOH£©=2mol/L”Į1L=2mol£¬æÉÄÜĻČŗó·¢Éś·“Ó¦¢ŁCH4+2O2”śCO2+2H2O”¢¢ŚCO2+2KOH=K2CO3+H2O”¢¢ŪK2CO3+CO2+H2O=2KHCO3£»øł¾Ż¼×ĶéµÄĮæ¼ĘĖćÉś³ÉµÄ¶žŃõ»ÆĢ¼µÄĮ棬½įŗĻ·“Ó¦·½³ĢŹ½ÅŠ¶Ļ·“Ó¦²śĪļ¼°£®
½ā“š ½ā£ŗ£Ø1£©Č¼ĮĻµē³ŲÖŠ£¬ĶØČėCH4µÄŅ»¶Ė£ØA£©ĪŖŌµē³ŲµÄøŗ¼«£¬ČÜŅŗÖŠOH-Ļņøŗ¼«ĒųŅĘ¶Æ£¬
¹Ź“š°øĪŖ£ŗA£»A£»
£Ø2£©µ±0£¼V”Ü22.4LŹ±£¬0£¼n£ØCH4£©”Ü1mol£¬Ōņ0£¼n£ØCO2£©”Ü1mol£¬Ö»·¢Éś·“Ó¦¢Ł¢Ś£¬ĒŅKOH¹żĮ棬Ōņµē³Ų×Ü·“Ó¦Ź½ĪŖCH4+2O2+2KOH=K2CO3+3H2O£¬
¹Ź“š°øĪŖ£ŗCH4+2O2+2KOHØTK2CO3+3H2O£»
£Ø3£©µ±V=33.6LŹ±£¬n£ØCH4£©=1.5mol£¬n£ØCO2£©=1.5mol£¬Ōņµē³Ų×Ü·“Ó¦Ź½ĪŖ3CH4+6O2+4KOH=K2CO3+2KHCO3+7H2O£¬ŌņµĆµ½0.5molK2CO3ŗĶ1molKHCO3µÄČÜŅŗ£¬ĪļÖŹµÄĮæÖ®±ČĪŖ£ŗ1£ŗ2£¬
¹Ź“š°øĪŖ£ŗK2CO3ŗĶKHCO3£»1£ŗ2£®
µćĘĄ ±¾Ģāæ¼²éĮĖČ¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķ£¬×¢Ņā¶žŃõ»ÆĢ¼Óėµē½āÖŹĒāŃõ»Æ¼Ų·“Ó¦ĮæµÄÅŠ¶Ļ£¬¼ĘĖćŅŖĒóµÄ×ŪŗĻŠŌ½ĻĒ棬ÄŃ¶Č½Ļ“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ūŗĻĶ¬Ņ»ĶØŹ½µÄÓŠ»śĪļŅ»¶Ø»„ĪŖĶ¬ĻµĪļ | |
| B£® | ŅŅĶé²»ÄÜŹ¹äåĖ®ŗĶøßĆĢĖį¼ŲĖįŠŌČÜŅŗĶŹÉ« | |
| C£® | ĖłÓŠµÄÓŠ»śĪļ¶¼ŗÜČŻŅ×Č¼ÉÕ | |
| D£® | Ņ×ČÜÓŚĘūÓĶ”¢¾Ę¾«”¢±½µČÓŠ»śČܼĮÖŠµÄĪļÖŹŅ»¶ØŹĒÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł | B£® | ¢Ś | C£® | ¢Ū | D£® | ¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ӧɜ³É67.2LH2Ź±£¬×ŖŅʵĵē×ÓŹżĪŖ9NA | |
| B£® | 2L0.5mol/L“×ĖįÄĘČÜŅŗÖŠŗ¬CH3COO-øöŹżŠ”ÓŚNA | |
| C£® | 28gCOŗĶC2H4µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄĢ¼Ō×Ó×ÜŹżĪŖ1.5NA | |
| D£® | 2molSO2Óė2molO2ŌŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó£¬ČŻĘ÷ÄŚµÄĘųĢå·Ö×ÓŹżĪŖ3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®ČÜŅŗÖŠ£ŗK+”¢Ca2+”¢C1-”¢NO${\;}_{3}^{-}$ | |
| B£® | æÕĘų£ŗCH4”¢CO2”¢SO2”¢NO | |
| C£® | ĒāŃõ»ÆĢś½ŗĢå£ŗH+”¢K+”¢S2-”¢Br- | |
| D£® | øßĆĢĖį¼ŲČÜŅŗ£ŗH+”¢Na+”¢SO${\;}_{4}^{2-}$”¢I- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®ĆŗĘų | B£® | ½¹ĀÆĆŗĘų | C£® | ŹÆÓĶŅŗ»ÆĘų | D£® | øßĀÆĆŗĘų |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com