
 ;MgF2
;MgF2 .
. 和
和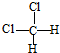
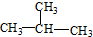
分析 (1)在阳离子中,质量数=质子数+中子数;核电荷数=质子数=核外电子数+所带电荷数;
(2)H2S是硫原子和氢原子之间通过共价键形成的共价化合物,MgF2是镁离子和氟离子之间通过离子键形成的离子化合物;
(3)四氧化三铁铝热法炼铁是利用铝热反应,铝和四氧化三铁高温反应生成铁和氧化铝,电解法冶炼铝氧化铝熔融通电电解得到金属铝和氧气;
(4)根据结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
分子式相同,结构不同的化合物互称为同分异构体;
质子数相同中子数不同的原子互称同位素;
同种物质指组成和结构都相同的物质;根据以上概念进行判断.
解答 解:(1)因2311Na+的质子数为11,质量数为23,中子数=质量数-质子数=23-11=12,核外电子数=质子数-所带电荷数=11-1=10,
故答案为:11;12;10;
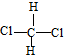
(2)H2S是硫原子和氢原子之间通过共价键形成的共价化合物,形成过程为
MgF2是镁离子和氟离子之间通过离子键形成的离子化合物,形成过程为 ,
,
故答案为: ;
; ;
;
(3)四氧化三铁铝热法炼铁是利用铝热反应,铝和四氧化三铁高温反应生成铁和氧化铝,反应的化学方程式为:3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,电解法冶炼铝氧化铝熔融通电电解得到金属铝和氧气,反应的化学方程式为:2A2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
故答案为:3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,2A2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
(4)①A.${\;}_6^{12}$C和${\;}_6^{14}$C,C的中子数不同,是碳元素的不同原子,互为同位素,
故答案为:A;
②B.CH3CH2CH2CH3和  结构相似,都属于烷烃,分子组成相差1个CH2原子团,互为同系物,
结构相似,都属于烷烃,分子组成相差1个CH2原子团,互为同系物,
故答案为:B;
C. 和
和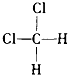 组成和结构都相同,为同一物质,
组成和结构都相同,为同一物质,
③D. 分子式相同,结构不同,为同分异构体,
分子式相同,结构不同,为同分异构体,
故答案为:D.
点评 本题考查离子中粒子数目的关系、用电子式的形成过程\同系物、同分异构体、同位素、同素异形体、同一物质的区别,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:推断题
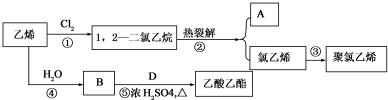
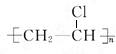 ,该反应类型是加聚反应
,该反应类型是加聚反应查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若要测定所得硫酸铜晶体中结晶水的数目,实验中要用到坩埚、坩埚钳和干燥器等 | |
| B. | 利用Cu(OH)2替代CuO也可调试溶液pH,不影响实验结果 | |
| C. | 洗涤晶体:向滤出晶体的漏斗中加少量冷水浸没晶体,自然流下,重复2-3次 | |
| D. | 用18.4mol/L浓硫酸配制溶解所用4.00mol/L的稀硫酸,玻璃仪器一般只有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
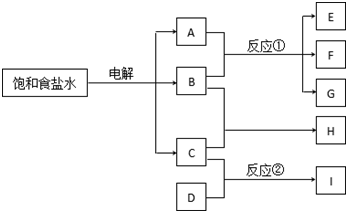 下列每一方框中的字母代表一种反应物或生成物:
下列每一方框中的字母代表一种反应物或生成物:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该晶体属于原子晶体,其化学键比金刚石中的更牢固 | |
| B. | 该晶体中碳原子和氮原子的最外层都满足8电子结构 | |
| C. | 该晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子 | |
| D. | 该晶体与金刚石相似,都是原子间以非极性共价键形成空间网状结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×(10-14+10-10)mol•L-1 | B. | $\frac{1×{(10}^{-14}{+10}^{-10})}{2}$mol•L-1 | ||
| C. | 2×10-10mol•L-1 | D. | 2×10-14mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40℃时同浓度的H2O2的分解速率一定比10℃时分解速率快 | |
| B. | 实验室用氯酸钾制氧气,增大压强可使反应速率加快 | |
| C. | 改变固体表面积对化学反应速率没有影响 | |
| D. | 在可逆反应中,因受反应限度的影响,研究改变外界条件来提高产率是没有意义的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双键、三键中一定含有π键 | |
| B. | 成键原子间原子轨道重叠越多,共价键越牢固 | |
| C. | 因每个原子未成对电子数是一定的,故配对原子个数也一定 | |
| D. | 每一个原子轨道在空间都具有方向性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HF>HCl>HBr>HI | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性:H2SO4>H3PO4>HClO4 | D. | 氧化性:O2>S>Se |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com