
| c(H+) |
| c(OH-) |
| c(H+) |
| c(HA) |
| c(HA) |
| c(A-) |
| c(H+) |
| c(OH-) |
| c(H+) |
| c(OH-) |
| c(H+) |
| c(OH-) |
| 10-1mol/L |
| 10-13mol/L |
| c(H+) |
| c(OH-) |
| c(H+) |
| c(HA) |
| c(H+)c(A-) |
| c(HA)c(A-) |
| Ka |
| c(A-) |
| c(HA) |
| c(A-) |
| c(HA)c(H+) |
| c(A-)c(H+) |
| c(H+) |
| Ka |
| 0.003��0.05-0.001��0.05 |
| 0.1 |
| 10-12 |
| 0.001 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
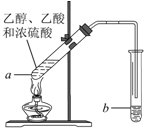 �����Ѿ��ܷⴢ��ʱ��Խ��������Խ�ã�ԭ��֮һ�Ǵ������������������ζ��������ʵ����Ҳ��������ͼ��ʾ��װ����ȡ������������ش��������⣮
�����Ѿ��ܷⴢ��ʱ��Խ��������Խ�ã�ԭ��֮һ�Ǵ������������������ζ��������ʵ����Ҳ��������ͼ��ʾ��װ����ȡ������������ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
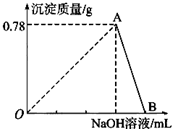 ��20mL AlCl3��Һ�е���2mol?L-1NaOH��Һʱ���������������μ�NaOH��Һ�����mL����ϵ��ͼ��ʾ��
��20mL AlCl3��Һ�е���2mol?L-1NaOH��Һʱ���������������μ�NaOH��Һ�����mL����ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
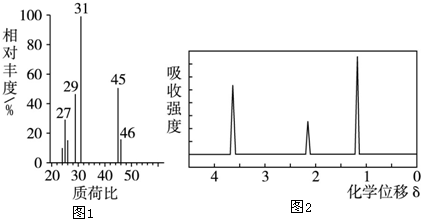 Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺
Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��WX2��YX2���γɵľ���������ͬ |
| B��WX2��ZX2�Ļ�ѧ��������ͬ�����Ӽ��Բ���ͬ |
| C��WX2����������ԭ������㶼��8���ӽṹ |
| D��ԭ�Ӱ뾶��С˳��ΪX��W��Z��Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��500mL 1mol?L-1 MgCl2��Һ�к���Cl-��ĿΪ0.5NA |
| B����״���£�1mol H2O��1mol O2��ռ�������� |
| C��17g NH3���еĵ��Ӹ���Ϊ10NA |
| D��36g H2O��32g CH4��������ԭ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com