
碳、硫的含量影响钢铁性能,碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2。

①气体a的成分是________________。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2 1________+3________。
1________+3________。
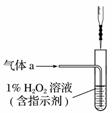
(2)将气体a通入测硫装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式
________________________________________________________________________
________________________________________________________________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液,若消耗1 mL NaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。
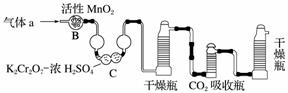
①气体a通过B和C的目的是______________________________________。
②计算钢样中碳的质量分数,应测量的数据是________________________________________________________________________
________________________________________________________________________
解析 (1)①钢样(含有铁、碳、硫)在高温下与O2反应,除生成CO2、SO2外,还有剩余的O2,故气体a中含有CO2、SO2、O2。
②该反应中,S元素由-2价被氧化为+4价,即生成SO2,再结合元素守恒及元素的化合价升降总数相等,配平该反应方程式:3FeS+5O2 Fe3O4+3SO2。
Fe3O4+3SO2。
(2)①H2O2具有强氧化性,SO2具有强还原性,二者发生氧化还原反应生成H2SO4,化学方程式为H2O2+SO2===H2SO4。
②消耗1 mL NaOH溶液相当于硫的质量为y g,则消耗z mL NaOH溶液相当于硫的质量为yz g,那么钢样中硫的质量分数为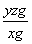 =
=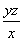 。
。
(3)①装置B中活性MnO2将SO2氧化。装置C中K2Cr2O7浓H2SO4具有强氧化性,用于吸收气体a中的SO2,防止SO2进入CO2吸收瓶,影响实验结果。
②实验中应测定实验前后CO2吸收瓶的质量变化,从而确定CO2的质量,继而求出钢样中碳的质量分数。
答案 (1)①SO2、CO2、O2 ②Fe3O4 SO2
(2)①H2O2+SO2===H2SO4 ②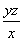
(3)①排除SO2对CO2测定的干扰 ②CO2吸收瓶吸收CO2前、后的质量


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒沙特列原理来解释的是
A.加压有利于SO2与O2反应生成SO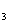
B.密闭容器中发生反应H2(g)+I2(g) 2HI(g),增大压强时容器中颜色加深。
2HI(g),增大压强时容器中颜色加深。
C.将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应
D.用过量氮气与氢气反应可以提高氢气的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①常温下,0.1 mol·L-1某一元酸(HA)溶液中 =1×10-8,由水电离出的c(H+)=1×10-11 mol·L-1
=1×10-8,由水电离出的c(H+)=1×10-11 mol·L-1
②浓度为0.1mol·L-1的某酸式盐NaHA溶液中c(Na+) =c(A2-)+c(HA-) +c(H2A)
③pH=12的氨水与pH=2的盐酸等体积混合c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④浓度均为0.1mol·L-1的小苏打溶液与烧碱溶液等体积混合
c(Na+)+c(H+)=2c(CO32-)+c(OH-)
A.①②③ B.①②④ C.①③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
|
|
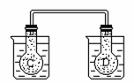 如右图所示,在常温下容器 A 中盛有 500mL 蒸馏水,在容器 B 中盛有 500ml 1mol/L的盐酸,在烧瓶 C 和 D 中充满二氧化氮气体,并用导管将它们连通。向 A 容器中加入 50g 硝酸铵晶体,小心搅拌,使其迅速溶
如右图所示,在常温下容器 A 中盛有 500mL 蒸馏水,在容器 B 中盛有 500ml 1mol/L的盐酸,在烧瓶 C 和 D 中充满二氧化氮气体,并用导管将它们连通。向 A 容器中加入 50g 硝酸铵晶体,小心搅拌,使其迅速溶 解;向B中加入 10g 苛性钠固体,小心搅拌也使其迅速溶解,随着A、B中固体物质的溶解,烧瓶 C 和 D 中气体的颜色变化是____ __ 。
① 不变 ② 烧瓶 C 中颜色变深,D 中变浅
③ 烧瓶 D 中 变深, C 中变浅 ④ 两个烧瓶中的颜色都变深
查看答案和解析>>
科目:高中化学 来源: 题型:
0.80 g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
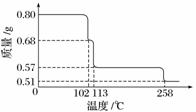
请回答下列问题:
(1)试确定200 ℃时固体物质的化学式______________________________________;
(要求写出推断过程)。
(2)取270 ℃所得样品,于570 ℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为________________________;把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为________,其存在的最高温度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素 ( )
A.在自然界中只以化合态的形式存在
B.单质常用作半导体材料和光导纤维
C.最高价氧化物不与酸反应
D.气态氢化物比甲烷稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com