
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
| A、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
| B、常温下,1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、将AlCl3溶液加热蒸干并灼烧后剩余固体为Al2O3 |
| D、常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,则此溶液可能是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
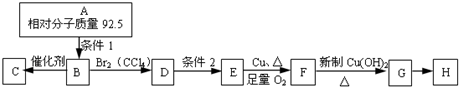
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和碘水和CCl4加入分液漏斗中后,塞上上口部的玻璃塞,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡 |
| B、静置,分液漏斗中溶液分层,下层呈紫红色上层几乎无色 |
| C、打开分液漏斗的活塞使下层液体沿烧杯内壁慢慢流出 |
| D、下层液体流完后继续打开活塞另用容器接收上层液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁 | B、铝 | C、锌 | D、铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
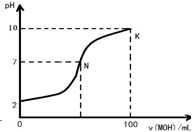 常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
| C、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001 mol?L-1 | ||
D、随着MOH溶液的滴加,比值
|
查看答案和解析>>
科目:高中化学 来源: 题型:
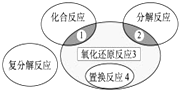
A、2H2+O2
| ||||
| B、Zn+H2SO4=ZnSO4+H2↑ | ||||
C、CuO+CO
| ||||
D、2NaHCO3
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com