
| A.热稳定性:H2Se> H2S> HCl | B.原子半径:Se>P>Si |
| C.酸性:H3PO4>H2SO4>H2SeO4 | D.还原性:Se2->Br->Cl- |
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Be<B<C<N |
| B.第一电离能:B<Be<Mg<Na |
| C.元素的电负性:O>N>P>Si |
| D.气态氢化物的稳定性:NH3<CH4<PH3<SiH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属元素和非金属元素间形成的化学键一定是离子键 |
| B.ⅦA族元素是同周期元素中非金属性最强的元素 |
| C.全部由非金属元素形成的化合物一定是共价化合物 |
| D.短周期中,同周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| W | X | |
| | Y | Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
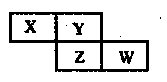
| A.最简单气态氢化物的热稳定性:Y>Z |
| B.最高价氧化物的水化物的酸性:X<W |
| C.X元素的氢化物与其最高价氧化物的水化物能形成离子化合物 |
| D.Y的氢化物沸点远高于Z的氢化物,是因为H-Y键的键能高于H-Z键的键能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c>b>a | B.a>b>c | C.a>c>b | D.c>a>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠和镁分别与冷水反应,判断钠和镁的金属活动性强弱 |
| B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱 |
| C.硫酸和硅酸钠溶液反应出白色沉淀,判断硫与硅的非金属活动性强弱 |
| D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子最外层电子数大于3(小于8)的元素一定是非金属元素 |
| B.原子最外层只有1个电子的元素一定是金属元素 |
| C.最外层电子数比次外层电子数多的元素一定位于第2周期 |
| D.某元素的离子的最外层与次外层电子数相同,该元素一定位于第3周期 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com