
能正确表示下列反应的离子方程式的是( )
A.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H 2O
2O
C.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑
D.将铜屑加入含Fe3+的溶液中:2Fe3++Cu=2Fe2++Cu2+
科目:高中化学 来源: 题型:
有M、N两种溶液, 经测定这两种溶液中含有下列12种离子:Al3+、Cl-、Na+、K+、NO
经测定这两种溶液中含有下列12种离子:Al3+、Cl-、Na+、K+、NO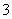 、OH-、Fe2+、[Al(OH)4]-、CO
、OH-、Fe2+、[Al(OH)4]-、CO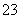 、NH
、NH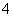 、SO
、SO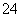 、H+。
、H+。
(1)完成下列表格中实验①的结论和实验②的实验内容以及现象:
| 实验内容以及现象 | 结论 |
| ①取少量N溶液滴加足量的硝酸钡溶液,无沉淀产生 | |
| ② | 确定M溶液中含有Na+,不含K+ |
|
|
(2)根据(1)中的实验回答:
NO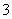 存在于________溶液中,理由是_______________________________________;
存在于________溶液中,理由是_______________________________________;
Cl-存在于________溶液中,理由是________________________________________。
(3)根据(1)中的实验确定,M溶液中含有的离子为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是 ( )
A.用过量氨水吸收工业尾气中的SO2:2NH3·H20+SO2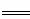 2NH4++SO32-+H2O
2NH4++SO32-+H2O
B.氯化钠与浓硫酸混合加热:H2SO4+2Cl- SO2↑+Cl2↑+H2O
SO2↑+Cl2↑+H2O
C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:
2Ba2++3OH-+Al3++2SO42- 2BaSO4↓+Al(OH)3↓
2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是 ( )
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:
Ba 2++2OH-+NH
2++2OH-+NH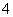 +HCO
+HCO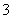 =BaCO3↓+NH3·H2O+H2O
=BaCO3↓+NH3·H2O+H2O
B.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O
C.向亚硫酸钠溶液中加入足量硝酸:SO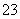 +2H+=SO2↑+H2O
+2H+=SO2↑+H2O
D.向AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH↓+NH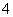
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是 ( )。
A.澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO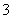 =CaCO3↓+CO
=CaCO3↓+CO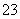 +2H2O
+2H2O
B.磁性氧化铁置于氢碘酸溶液中:Fe3O4+8HI=2Fe3++Fe2++4H2O+8I-
C.NaHSO4溶液中滴加过量Ba(OH)2溶液:H++SO +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O
D.醋酸与氨水混合:CH3COOH+NH3·H2O=CH3COONH4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子组在一定条件下不能大量共存,且所给离子方程式能说明不能共存原因的是( )
| 选项 | 条件 | 离子组 | 共存所发生的离子反应方程式 |
| A | pH=1的溶液 | Fe2+、Al3+、Cl-、MnO4- | 10Cl-+2MnO4-+16H+===2Mn2++5Cl2↑+8H2O |
| B | 常温下c(OH)-=10-2mol·L-1的能与金属铝反应放出氢气的溶液 | K+、NO3-、Cl-、NH4+ | NH4++OH-===NH3·H2O |
| C | 能使酚酞试液变红的溶液 | Na+、Cl-、S2-、SO32- | SO32-+2S2-+6H+===3S↓+3H2O |
| D | 含有大量H+的透明溶液 | Na+、Cu2+、AlO2-、SiO32- | 2H++SiO32-===H2SiO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA 为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA
B.78 g 苯含有C=C 双键的数目为3NA
C.常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6. 72 L NO2与水充分反应转移的电子数目为0. 1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G为原子序数依次递增的7种短周期主族元素。A、B元素的最高正价与最低负价的代数和均为零;C元素是植物生长三大营养元素之一;D的单质具有强氧化性,其氢化物能和一种半导体材料反应生成常温常压下的两种气体;E原子核外K层电子数与M层电子数相等;F原子的价电子数等于电子层数的两倍。请回答下列问题:
(1)CD3 的电子式为 ;
(2)用离子方程式表示G 的非金属性比F强 ;
(3)EF在空气中充分灼烧生成一种稳定性的盐,则此反应方程式为 ;
(4)C的氢化物与G的单质以物质的量之比1:3反应,生成二元化合物X和一种气体,该气体遇氨气产生“白烟”,则X的化学是为 ,X与水反应的产物名称是
;
(5)已知充分燃烧一定量的B2A2放出Q kJ的能量,燃烧生成的产物恰好与100ml 5 mol·L-1的NaOH溶液完全反应生成正盐,则燃烧1mol B2A2放出的热量为 KJ;
(6)常温下,E(OH)2在水中的沉淀溶解平衡曲线如图所示(单位mol·L-1)。要使c(E2+) 为0.001 mol·L-1的溶液形成沉淀,则溶液的PH值至少升高到 。


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com