
【题目】某物质只含C,H,O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键). 
(1)该物质的结构简式为
(2)该物质中所含官能团的名称为 .
(3)下列物质中,与该产品互为同系物的是(填序号) , 互为同分异构体的是 . ①CH3CH═CHCOOH ②CH2═CHCOOCH3
③CH3CH2CH═CHCOOH ④CH3CH(CH3)COOH.
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/gcm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
请回答下列问题: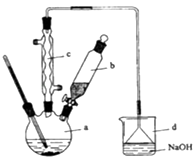
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白色烟雾产生,是因为生成了气体.继续滴加至液溴滴完.装置d的作用是;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 , 要进一步提纯,下列操作中必须的是(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KCl溶液中含有的少量K2SO4杂质得到纯的KCl,选用的最佳试剂及顺序为( )
①BaCl2 ②Ba(NO3)2 ③K2CO3 ④Na2CO3 ⑤HCl ⑥HNO3
A.①②B.①③⑤C.②③⑥D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠溶液含有少量的氯化铁。若要得到纯净的固体氯化钠,可供选择的操作有:①加适量盐酸溶液、②加金属铁粉、③蒸发结晶、④加过量氢氧化钠溶液、⑤冷却热饱和溶液、⑥过滤。正确的操作步骤是( )
A. ②⑥③B. ④⑥①③C. ④⑥③⑤D. ②⑥①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在玻璃中加入溴化银(AgBr)和氧化铜可制得变色镜片,其中所含物质及变色原理如图所示,下列说法不正确的是( )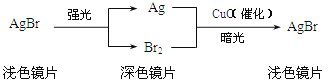
A.溴化银应避光保存
B.变色镜片可反复变色
C.变色镜片颜色变深的过程发生了化合反应
D.变色镜片中的氧化铜在变色过程中质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁子香酚的结构简式如图所示: 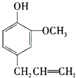 .丁子香酚的一种同分异构体对甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体.某校兴趣小组提出可以利用中学所学的简单有机物合成F,其方案如下,其中A的产量标志着一个国家石油化学工业的发展水平.
.丁子香酚的一种同分异构体对甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体.某校兴趣小组提出可以利用中学所学的简单有机物合成F,其方案如下,其中A的产量标志着一个国家石油化学工业的发展水平. 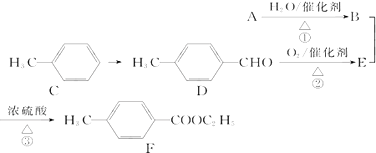
(1)写出丁子香酚的分子式 . 写出C物质的名称 .
(2)指出化学反应类型:反应① . 反应② .
(3)下列物质不能与丁子香酚发生反应的是 . a.NaOH溶液 b.NaHCO3溶液
c.Br2的四氯化碳溶液 d.乙醇
(4)写出反应③的化学方程式:
(5)写出符合条件①含有苯环;②能够发生银镜反应的D的同分异构体的结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,体积相同、pH均为3的醋酸和硫酸的说法正确的是( )
A.分别加入足量锌片,两种溶液生成H2的体积相同
B.分别加水稀释100倍后,两种溶液的pH仍相同
C.醋酸中的c(CH3COO﹣)和硫酸中的c(SO ![]() )相等
)相等
D.两种溶液中,由水电离出的氢离子浓度均为1×10﹣11 mol?L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2分别通入下列4种溶液中,有关说法正确的是
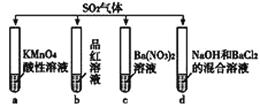
A. 试管a中实验可以证明SO2具有漂白性
B. 试管b中溶液褪色,说明SO2具有强氧化性
C. 试管c中能产生白色沉淀,该沉淀的成分为BaSO3
D. 试管d中能产生白色沉淀,该沉淀完全溶于稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其中溶液的pH变化是判断滴定终点的依据.
实验 | 消耗0.1000molL﹣1的 | 待测氢氧化钠 |
1 | 29.02 | 25.00 |
2 | 28.01 | 25.00 |
3 | 27.99 | 25.00 |
(1)如图所示A的pH范围使用的指示剂是;
(2)用0.1000molL﹣1的盐酸溶液滴定未知浓度的氢氧化钠溶液,重复三次的实验数据如表所示.则待测氢氧化钠的物质的量浓度是molL﹣1 . 在上述滴定过程中,若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将(填“偏高”、“偏低”或“不影响”).
(3)下列关于上述中和滴定过程中的操作正确的是(填序号)
A.用碱式滴定管量取未知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待盛放液润洗
C.滴定中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com