
【题目】一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)![]() 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
A. 2.5mol C B. 2 mol A、2 mol B和10 mol He(不参加反应)
C. 1.5 mol B和1.5 mol C D. 2 mol A、3 mol B和3 mol C
【答案】A
【解析】
反应2A(g)+B(g)3C(g)中,气体的体积前后相同,在一定温度下,在恒容密闭容器中得到平衡状态,只要满足物质全部转化为A、B,且满足n(A):n(B)=1:1,即可得到相同平衡状态,结合浓度对平衡移动的影响,只要加入的物质的量:n(A):n(B)>1:1,平衡后A的体积分数大于a%。
反应2A(g)+B(g)3C(g)中,气体的体积前后相同,在一定温度下,在恒容密闭容器中得到平衡状态,只要满足物质全部转化为A、B,且满足n(A):n(B)=1:1,就是等效平衡,结合浓度对平衡移动的影响,只要加入的物质的量:n(A):n(B)>1:1,平衡后A的体积分数大于a%,A.2molC相当于![]() molA和
molA和![]() molB,二者的比值为2:1,大于1:1,则平衡后A的体积分数大于a%,选项A正确;B.2molA、2molB和1molHe(不参加反应),n(A):n(B)=2:2,等于1:1,则平衡后A的体积分数等于a%,选项B错误;
molB,二者的比值为2:1,大于1:1,则平衡后A的体积分数大于a%,选项A正确;B.2molA、2molB和1molHe(不参加反应),n(A):n(B)=2:2,等于1:1,则平衡后A的体积分数等于a%,选项B错误;
C.1molB和1molC,相当于![]() molA和
molA和![]() molB,n(A):n(B)=1:2,小于1:1,则平衡后A的体积分数小于a%,选项C错误;D.2molA、3molB和3molC,相当于4molA和4molB,二者的比值为4:4,等于1:1,则平衡后A的体积分数等于a%,选项D错误,答案选A。
molB,n(A):n(B)=1:2,小于1:1,则平衡后A的体积分数小于a%,选项C错误;D.2molA、3molB和3molC,相当于4molA和4molB,二者的比值为4:4,等于1:1,则平衡后A的体积分数等于a%,选项D错误,答案选A。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是

A. a电极是负极
B. b电极的电极反应为:4OH--4e-====2H2O+O2↑
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向某二元弱酸H2X的钠盐溶液中滴加盐酸,混合溶液中离子浓度与pH的关系如图所示,其中lgX = ![]() 或
或![]() 。下列叙述不正确的是
。下列叙述不正确的是

A. 曲线m表示![]() 与pH的变化关系
与pH的变化关系
B. Ka1(H2X)的数量级为10-7
C. 当溶液呈中性时, c(HX-)>c(X2-)>c(H2X)
D. 25℃时,NaHX溶液中:c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
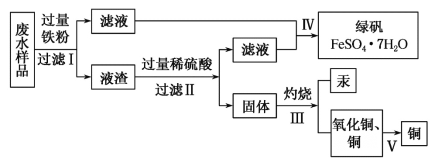
(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是__________设计简单实验检验绿矾是否变质,简述你的操作:__________。
(2)步骤Ⅰ中加入过量铁粉的目的是__________,步骤Ⅱ中__________(填“能”或“不能”)用盐酸代替硫酸。
(3)步骤V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案__________不好;从产品纯度考虑,方案__________不好。
(4)写出步骤Ⅱ中涉及反应的离子方程式:__________;步骤Ⅳ得到绿矾的操作蒸发浓缩__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)![]() 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a molA,同时生成3a mol B
⑧A、B、C的分子数之比为1:3:2
A. ⑤⑥B. ⑦④C. ①③D. ②⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼钛的有关反应如下所示:
① C(s) + O2(g) ![]() CO2(g) ΔH1
CO2(g) ΔH1
② 2CO(g) + O2(g) ![]() 2CO2(g) ΔH2
2CO2(g) ΔH2
③ TiO2(s) + 2Cl2(g) ![]() TiCl4(g) + O2(g) ΔH3
TiCl4(g) + O2(g) ΔH3
④ TiCl4(s) + 2Mg(s) ![]() 2MgCl2(s) + Ti(s) ΔH4
2MgCl2(s) + Ti(s) ΔH4
⑤ TiO2(s) + 2Cl2(g) + 2C(s) ![]() TiCl4(g) + 2CO(g) ΔH5
TiCl4(g) + 2CO(g) ΔH5
下列有关推断正确的是( )
A. 2ΔH1=ΔH2 B. ΔH1<0,ΔH2>0
C. ΔH5=ΔH3+2ΔH1-ΔH2 D. 2ΔH1-ΔH2>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示装置的叙述错误的是
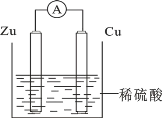
A. 锌是负极,其质量逐渐减小
B. 氢离子在铜表面得e-
C. 电子从锌片经导线流向铜片
D. 电流从锌片经导线流向铜片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学选3——物质结构与性质)利用 合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
合成的新型三元催化剂[La0.8Cu0.2Ni1-xMxO3(M 分别为Mn、Fe和Co)]可以使汽车尾气中NO和CO发生反应而减少尾气污染,同时可大大降低重金属的用量。回答下列问题:
(1)Mn2+的核外电子排布式为:________________,其单电子数为_________________。
(2)C、N、O、Mn电负性由大到小的顺序是___________。
(3)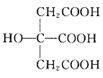 也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为_____。
也是常见配体,其中采取sp2杂化的碳原子和sp3杂化的碳原子个数比为_____。
(4)蓝色物质KFe(Ⅲ)x[Fe(Ⅱ)(CN)6]可缓解重金属中毒,x=_______;该物质中不存在的作用力有_____。
A.范德华力 B.离子键 C.σ键 D.π键 E.氢键
(5)副族元素钴的氧化物可以在室温下完全氧化甲醛(HCHO)。甲醛分子的立体构型为_____;甲醛常温下为气体而甲醇(CH3OH)为液体的原因是________________________________ 。
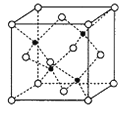
(6)副族元素Mn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中(○为Se,![]() 为Mn),该化合物的化学式为________,Se的配位数为______,Mn和Se的摩尔质量分别为M1g/mol、M2g/mol,该晶体的密度为ρg/cm3,则Mn—Se键的键长为_____________nm(计算表达式)。
为Mn),该化合物的化学式为________,Se的配位数为______,Mn和Se的摩尔质量分别为M1g/mol、M2g/mol,该晶体的密度为ρg/cm3,则Mn—Se键的键长为_____________nm(计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能说明反应X(g)+2Y(g)![]() 2Z(g)达到化学平衡状态的是
2Z(g)达到化学平衡状态的是
A. X、Y、Z的物质的量之比为1:2:2B. X、Y、Z的浓度不再发生变化
C. 反应速率v(X)= v(Y)D. 单位时间内生成n mol Z的同时生成2n mol Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com