
| A. | 乙酸 | B. | 乙醛 | C. | 甲酸乙酯 | D. | 乙醇 |
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe3++Cu | |
| B. | NaHSO4溶液与氢氧化钠溶液反应:OH-+H+═H2O | |
| C. | 氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与盐酸反应:CaCO3+2H+═H2O+CO2↑+Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业合成氨 | |
| B. | 雷雨闪电时,大气中产生了一氧化氮 | |
| C. | 豆科作物的根瘤菌将空气中的氮转化为氨 | |
| D. | 在一定条件下由氨气和二氧化碳合成尿素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
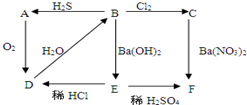 图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.
图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
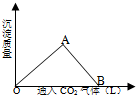 (1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.
(1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com