
【题目】“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视,所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
______ C+______ KMnO4+______H2SO4→______CO2↑+______MnSO4+______K2SO4+______H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1条件下平衡常数K=_________(取小数二位,下同)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则![]() 的值_________(填具体值或取值范围)。
的值_________(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入10molCO,5molH2O,2molCO2,5molH2,则此时V正________V逆 (填“<”,“>”,“=”)
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
③H2O(g)=H2O(l) △H=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_______________。
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为_______________。
【答案】(12分)
(1) 5:4:6:5:4:2:6;
(2)2.67 0<![]() <1 <
<1 <
(3)CH3OH(I)+O2(g)=CO(g)+2H2O(I) △H=-442.8kJ·mol-1
(4)5.6×10-5
【解析】
试题分析:(1)根据氧化还原反应氧化剂、还原剂得失电子数目相等配平,反应中C元素化合价0→+4,Mn元素化合价+7→+2,反应得失电子相等,则有:5C~4KMnO4,根据质量守恒可确定H2SO4的计量数为6,则配平后的计量数分别是:5、4、6、5、4、2、6;
(2)① H2O(g)+CO(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度 1mol/L 2mol/L 0 0
转化浓度 0.8mol/L 0.8mol/l 0.8mol/l 0.8mol/l
平衡浓度 0.2mol/L 1.2mol/L 0.8mol/l 0.8mol/l
所以平衡常数K=![]() =2.67
=2.67
②增大水蒸气的浓度可以提高CO的转化率,因此实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是a<b,故0<![]() <1。
<1。
③实验2条件下平衡常数,需要列式计算平衡浓度
H2O(g)+CO(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度 0.5mol/L 1mol/L 0 0
转化浓度 0.2mol/L 0.2mol/l 0.2mol/l 0.2mol/l
平衡浓度 0.3mol/L 0.8mol/L 0.2mol/l 0.2mol/l
则K=![]() =0.17
=0.17
若在9000C时,另做一组实验,在此容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时![]() =0.2>0.17,这说明反应在向逆反应方向进行,因此υ正<υ逆。
=0.2>0.17,这说明反应在向逆反应方向进行,因此υ正<υ逆。
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
③H2O(g)=H2O(g) △H=-44.0kJ/mol
根据盖斯定律,将已知反应![]() ×(①-②+③×4)得到CH3OH(l)+O2(g)=CO(g)+2H2O(I),所以该反应的△H=
×(①-②+③×4)得到CH3OH(l)+O2(g)=CO(g)+2H2O(I),所以该反应的△H=![]() ×[(-1275.6kJ/mol)-(-566.0kJ/mol)+(-44.0kJ/mol)×4]=-442.8kJ·mol-1,
×[(-1275.6kJ/mol)-(-566.0kJ/mol)+(-44.0kJ/mol)×4]=-442.8kJ·mol-1,
即CH3OH(I)+O2(g)=CO(g)+2H2O(I) △H=-442.8kJ·mol-1。
(4)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=1/2×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)×c(Ca2+)=2.8×10-9可知,c(Ca2+)=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L。


科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法,错误的是( )
A.二氧化硫常用于漂白纸浆 B.漂粉精可用于游泳池水消毒
C.晶体硅常用于制作光导纤维 D.氧化铁常用于红色油漆和涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各题:
(1)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是__________
(2)将2.3 g 金属钠投入到2.0 mol/L 100 mL的MgCl2溶液中,完全反应后,所得溶液中Mg2+的物质的量浓度为__________(假定反应后溶液体积不变);如果将钠、镁、铝均为0.3 mol分别与100 mL浓度为1 mol/L的HCl溶液反应,产生氢气的体积比为____________。
(3)某溶液中只含有Na+、Al3+、Cl-、SO42-四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和SO42-的离子个数比为__________。
(4)青铜是人类历史上的一项伟大发明。工业冶炼铜的原理主要是:
(Ⅰ)2Cu2S(硫化亚铜)+3O2![]() 2Cu2O+2SO2↑
2Cu2O+2SO2↑
(Ⅱ)2Cu2O(氧化亚铜)+Cu2S![]() 6Cu+SO2↑
6Cu+SO2↑
①用“单线桥法”表示出上述反应(Ⅰ)中电子转移的方向和数目。
2Cu2S(硫化亚铜)+3O2![]() 2Cu2O+2SO2↑
2Cu2O+2SO2↑
②该反应(Ⅰ)中的还原产物是____________;反应(Ⅱ)中被氧化的物质是____________。
③若反应(Ⅰ)和反应(Ⅱ)均转移的电子数为1.806×1024,则在标准状况下产生的二氧化硫的体积为_____________ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于放热的氧化还原反应的是
A.二氧化碳与赤热的炭反应生成一氧化碳 B.葡萄糖在人体内氧化
C.生石灰制熟石灰 D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物、和水产资源等(如图所示),下列有关说法正确的是

A.第①步中除去粗盐中的SO42- 、Ca2+ 、Mg2+ 、Fe3+ 等杂质,加入的药品顺序为:
Na2CO3 溶液→NaOH溶液→BaCl2 溶液→过滤后加盐酸
B.工业上金属钠是通过氯碱工业制取
C.从第③步到第⑤步的目的是为了浓缩
D.在第③④⑤步中溴元素均被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液一定显酸性的是( )
A.溶液中c(OH-)>c(H+)
B.滴加紫色石蕊试液后变红色的溶液
C.溶液中c(H+)=10-6 mol/L
D.pH<7的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列有关说法正确的是
A. 聚氯乙烯塑料常用于食品保鲜膜
B. 研发使用高效催化剂,可提高可逆反应中原料的平衡转化率
C. 明矾可用于饮用水的净化,但不能杀菌消毒
D. 高纯度的硅单质广泛用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如下图所示,下列说法不正确的是
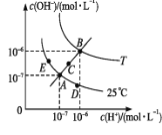
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com