
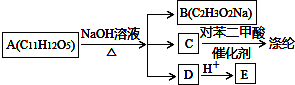


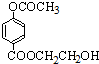 或
或
分析 涤纶的主要成分是聚对苯二甲酸乙二酯,根据C与对苯二甲酸反应生成涤纶可知,C应为HOCH2CH2OH,A与氢氧化钠溶液反应得B,根据B的分子式可知,B为CH3COONa,根据A的分子式和B、C的结构简式,且D酸化得E,E的苯环上一氯代物仅有两种,说明E中有两个取代基位于苯环的对位,所以D为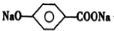 ,E为
,E为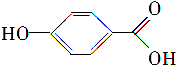 ,由B、C、D的结构简式可推知A为
,由B、C、D的结构简式可推知A为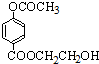 或
或 ,据此答题.
,据此答题.
解答 解:涤纶的主要成分是聚对苯二甲酸乙二酯,根据C与对苯二甲酸反应生成涤纶可知,C应为HOCH2CH2OH,A与氢氧化钠溶液反应得B,根据B的分子式可知,B为CH3COONa,根据A的分子式和B、C的结构简式,且D酸化得E,E的苯环上一氯代物仅有两种,说明E中有两个取代基位于苯环的对位,所以D为 ,E为
,E为 ,由B、C、D的结构简式可推知A为
,由B、C、D的结构简式可推知A为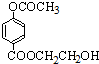 或
或 ,
,
(1)B为CH3COONa,B的化学名称为醋酸钠或乙酸钠,
故答案为:醋酸钠或乙酸钠;
(2)C为HOCH2CH2OH,由C合成涤纶的化学方程式为  ,
,
故答案为: ;
;
(3)根据上面的分析可知,E的结构简式为  ,
,
故答案为: ;
;
(4)根据上面的分析可知,A的结构简式 为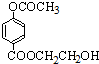 或
或 ,
,
故答案为: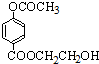 或
或 ;
;
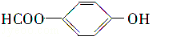
(5)E为 ,根据条件①核磁共振氢谱显示苯环上仅有两种氢,说明苯环上两个位于对位的基团,②可发生银镜反应和水解反应,说明有甲酸某酯,则符合条件的E的同分异构体的结构简式为
,根据条件①核磁共振氢谱显示苯环上仅有两种氢,说明苯环上两个位于对位的基团,②可发生银镜反应和水解反应,说明有甲酸某酯,则符合条件的E的同分异构体的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机推断,涉及酯、醇、醛、羧酸等性质以及学生推理能力等,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,难度中等,是高考热点题型.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 配制银氨溶液:在一定量2%的AgNO3溶液中滴加稀氨水至沉淀恰好溶解 | |
| B. | 除去混在苯中的少量苯酚:加入过量溴水,过滤 | |
| C. | 验证RX为碘代烷:把RX与烧碱水溶液混合加热,将溶液冷却后再加入硝酸银溶液 | |
| D. | 检验无水乙醇和浓硫酸共热后制得的气体是否为乙烯:将气体通入酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
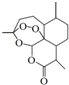 青蒿素是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物.其结构简式如图所示,则下列关于青蒿素的叙述正确的是( )
青蒿素是从植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯药物.其结构简式如图所示,则下列关于青蒿素的叙述正确的是( )| A. | 青蒿素易溶于水,难溶于乙醇和丙酮等溶剂 | |
| B. | 青蒿素的分子式为:C15H20O5 | |
| C. | 青蒿素因其具有“-O-O-”,所以具有一定的氧化性 | |
| D. | 青蒿素可以与NaOH、Na2CO3、NaHCO3发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

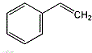 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
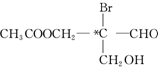 有光学活性.该有机物分别发生下列反应,生成的有机物仍有光学活性的是( )
有光学活性.该有机物分别发生下列反应,生成的有机物仍有光学活性的是( )| A. | 与乙酸发生酯化反应 | B. | 与NaOH水溶液反应 | ||
| C. | 与银氨溶液作用只发生银镜反应 | D. | 催化剂作用下与H2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | 用铝罐槽车储运浓硫酸 | 常温下,铝与浓硫酸不反应 |
| B | 在蔗糖中加入浓硫酸后出现发黑 | 浓硫酸具有脱水性 |
| C | 浓硝酸在光照下颜色变黄 | 浓HNO3不稳定,生成的有色产物NO2能溶于浓硝酸 |
| D | SO2能使溴水褪色 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的正极为锌 | |
| B. | 该电池的反应中二氧化锰起催化作用 | |
| C. | 当0.1 mol Zn完全溶解时,流经电解液的电子个数约为1.204×1023 | |
| D. | 电池的正极反应式为:2MnO2+2H2O+2e=2MnO(OH)+2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
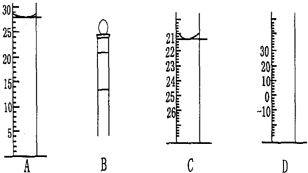
| 滴定序 号 | 待测液体积/mL | 所消耗盐酸标准液的体积/mL | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.52 | 25.02 |
| 2 | V | 0.40 | 24.40 | 24.00 |
| 3 | V | 1.00 | 25.98 | 24.98 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com