
如图所示是101 kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
A.1 mol H2中的化学键断裂时需要吸收436 kJ能量
B.2 mol HCl分子中的化学键形成时要释放862 kJ能量
C.此反应的热化学方程式为:H2(g)+Cl2(g)===2HCl(g)
ΔH=+183 kJ/mol
D.此反应的热化学方程式为: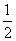 H2(g)+
H2(g)+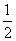 Cl2(g)===HCl(g) ΔH=-91.5 kJ/mol
Cl2(g)===HCl(g) ΔH=-91.5 kJ/mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知:2SO2(g)+O2(g)  2SO3(g) ΔH=-196 kJ·mol-1。
2SO3(g) ΔH=-196 kJ·mol-1。
(1)该反应的平衡常数表达式为K=________________;某温度下该反应的平衡常数K=10/3,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正)________v(逆)(填“<”“>”或“=”)
(2)一定温度下,向一带活塞的体积为2 L的密闭容器中充入2.0 mol SO2和1.0 mol O2,达到平衡后体积变为1.6 L,则SO2的平衡转化率为________。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是________(填字母)。
A.保持温度和容器体积不变,充入1.0 mol O2
B.保持温度和容器内压强不变,充入1.0 mol SO3
C.降低温度
D.移动活塞压缩气体
(4)若以如图所示装置,用电化学原理生产硫酸,写出通入SO2电极的电极反应式________________________________________________________________________。
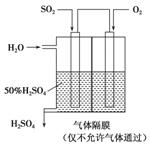
(5)为稳定持续生产,硫酸的浓度应维持不变,则通入SO2和水的质量比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产和生活密切相关,下列说法正确的是( )
A.甘油可用于配制化妆品
B.福尔马林可用于食品、标本、木材等的防腐
C.食品饮料中的菠萝酯,只能从菠萝中提取,不能通过有机合成生产
D.在野外,被黑蚂蚁蜇伤后,涂抹烧碱液可以缓解因注入皮肤内的蚁酸带的疼痛
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G、H、I、J均为有机化合物。根据以下框图,回答问题:
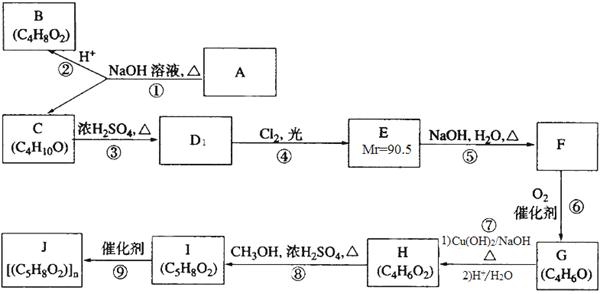
(1)④的反应类型是__________________,⑧的反应类型是__________________;
(2)B为有支链的有机化合物,B 的结构简式为______________________;C在浓硫酸作用下加热反应能生成三种烯烃:其中一种(D1)为“反—2—丁烯”;则另外两种(D2、D3)的结构简式分别为______________________、_____________________;
(3)A的分子式为:______________;J的结构简式为_____________________;
(4)写出下列反应的化学方程式:
反应⑤:_____________________________________________________;
反应⑦的第一步:_____________________________________________________;
(5)与H具有相同官能团的H的同分异构体的结构简式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又是吸热反应的是( )
A.铝与稀盐酸的反应
B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是
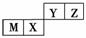 A.原子半径Z<M
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X 的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作或结论的叙述中不正确的是( )
|
|
|
|
|
| A.除去CO2中的HCl | B.溶液变红,待测液中含Fe3+ | C.有砖红色沉淀,葡萄糖中含醛基 | D.有白烟出现,浓盐酸有挥发性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是________________________。
(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:
Cr2O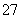 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
①在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、________和________。
②若滴定x mL滤液中的Fe2+,消耗a mol·L-1K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________mol·L-1。
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________(填序号)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4·2H2O。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
|
| A. | 1.0mol▪L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
|
| B. | 甲基橙呈红色的溶液:NH4+、Al3+、F﹣、Cl﹣ |
|
| C. | 某无色溶液中:Al3+、HCO3﹣、Cl﹣、Br﹣ |
|
| D. | pH=12的溶液:K+、Na+、CH3COO﹣、Ag(NH3)2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com