
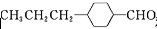 ��
��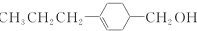 ��д�ṹ��ʽ�����ɣ�
��д�ṹ��ʽ�����ɣ�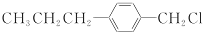 ��
��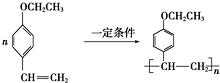 ��
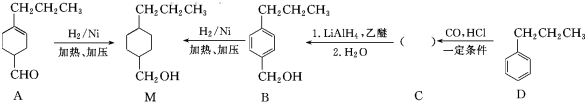
�� ���� ��1������M�Ľṹ��ʽȷ�������ʽ��
��2���л���A����ȩ��������ȩ�����ʣ�����̼̼˫��������ϩ�������ʣ�
��3�������л���A�Ľṹ��֪�����еĹ�����Ϊȩ����̼̼˫����
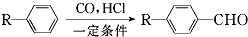
�Ա�D��B�Ľṹ��֪����Ϸ�Ӧ��Ϣ��֪��CΪ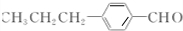 ��C������ԭ��Ӧ�õ�B��
��C������ԭ��Ӧ�õ�B��
��4��������ֻ��-CHO�����������ӳɷ�Ӧ��
��5��C����ȩ����B���д��ǻ�������ȩ��������Һ������������ͭ��Һ��Ӧ���飻
��6������BҲ����C10H13Cl��NaOHˮ��Һ�����Ƶã�����±������ˮ�ⷴӦ��B���ǻ���-Clȡ���ɵ�C10H13Cl�Ľṹ��ʽ��
��7��C��һ��ͬ���칹��E���������ص㣺a�������к�-OCH2CH3��b��������ֻ�����ֻ�ѧ������ͬ����ԭ�ӣ���EΪ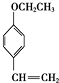 ��
��
��� �⣺��1������M�Ľṹ��ʽ����֪�����к���10��Cԭ�ӡ�20��Hԭ�ӡ�1��Oԭ�ӣ������ʽΪ��C10H20O��
�ʴ�Ϊ��C10H20O��
��2���л���A����ȩ��������ȩ�����ʣ�����̼̼˫��������ϩ�������ʣ�
a��ȩ����̼̼˫���������������ӳɷ�Ӧ��һ��������������2mol H2�����ӳɷ�Ӧ����a����
b������̼̼˫���������巢���ӳɷ�Ӧ��ȩ���ܱ�����������ʹBr2��CCl4��Һ��ɫ����b��ȷ��
c�����Ӻ���2��˫����������к���2���м�����c����
d������̼̼˫����ȩ������ʹ����KMnO4��Һ��ɫ����g��ȷ��
��ѡ��bd��
��3�������л���A�Ľṹ��֪�����еĹ�����Ϊȩ����̼̼˫�����Ա�D��B�Ľṹ��֪����Ϸ�Ӧ��Ϣ��֪��CΪ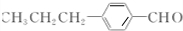 ��C������ԭ��Ӧ�õ�B��
��C������ԭ��Ӧ�õ�B��
�ʴ�Ϊ��ȩ����̼̼˫������ԭ��Ӧ��
��4��������ֻ��-CHO�����������ӳɷ�Ӧ�������⸱����ṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5��C����ȩ����B���д��ǻ�����������������Һ������������ͭ��Һ�����Ƿ���C��
�ʴ�Ϊ��������Һ������������ͭ��Һ��
��6������BҲ����C10H13Cl��NaOHˮ��Һ�����Ƶã�����±������ˮ�ⷴӦ��B���ǻ���-Clȡ���ɵ�C10H13Cl�Ľṹ��ʽΪ��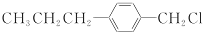 ��
��
�ʴ�Ϊ��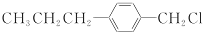 ��
��
��7��C��һ��ͬ���칹��E���������ص㣺a�������к�-OCH2CH3��b��������ֻ�����ֻ�ѧ������ͬ����ԭ�ӣ���EΪ ��E��һ�������·����Ӿ۷�Ӧ�Ļ�ѧ����ʽ��
��E��һ�������·����Ӿ۷�Ӧ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶ���ϳɡ������ŵĽṹ�����ʡ��л���Ӧ���͵ȣ��ѶȲ���ע�����չ����ŵ�������ת����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڿ�����ȼ��ʱ�����ȼ����С��ʹ��ѧƽ��������������SO3�ķ����ƶ� | |
| B�� | �ڴ�������ȼ��ʱ�����ȼ���ȴ����ڻ�ѧƽ��������SO3�ķ����ƶ� | |
| C�� | ����ȼ�յĹ����У�����SO3�����ɣ��¶ȵ�Ӱ���������Ũ�ȵ�Ӱ�� | |
| D�� | û��ʹ�ô��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2 mol Al������NaOH��Һ��Ӧ�����ɵ�H2���Ϊ6.72L | |
| B�� | ������pH=1��������Һ�е�H+������ĿΪ0.1NA | |
| C�� | Ǧ�����У�����������9.6gʱ����·��ͨ���ĵ�����ĿΪ0.3NA | |
| D�� | 11P4+60CuSO4+96H2O�T20Cu3P+24H3PO4+60H2SO4��Ӧ�У�6 mol CuSO4���������ķ�����Ϊ1.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£���Ӧ4Fe��OH��2��s��+2H2O��l��+O2��g���T4Fe��OH��3��s�����Է����У����H��0 | |
| B�� | ��Ƭ��пʱ����Ƭ�����Դ���������� | |
| C�� | ������NaClΪ����ʽ��е��ұ���ƣ���������Na+�������ƶ� | |
| D�� | t��ʱ�������ܱ������з�Ӧ��NO2��g��+SO2��g��?NO��g��+SO3��g����ͨ������O2��$\frac{c��NO��•c��S{O}_{3}��}{c��N{O}_{2}��•c��S{O}_{2}��}$��ֵ��SO2ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���� T/��n/mol T/�� | ����̿ | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �κ�����£��¶ȶ������ܶԷ�Ӧ�ķ�������������� | |
| B�� | pH=4��CH3COOH��NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ | |
| C�� | ��pH��ֽ�ⶨ��ҺpH����ȷ�����ǣ���һС����ֽ�ڴ���Һ��պһ�£�ȡ������ڱ������ϣ������ɫ������ | |
| D�� | pH=4.5�ķ���֭��c��H+����pH=6.5��ţ����c��H+����100�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
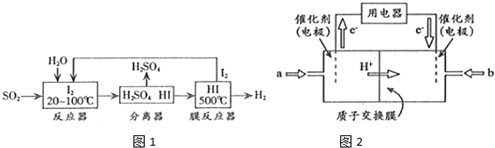
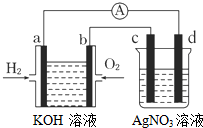 ����ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ�����ͼ��ʾ��ʵ�飨ͼ�����õ缫��Ϊ���Ե缫��������������ȷ���ǣ�������
����ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ�����ͼ��ʾ��ʵ�飨ͼ�����õ缫��Ϊ���Ե缫��������������ȷ���ǣ�������| A�� | a�缫�Ǹ�����OH-�������� | |
| B�� | b�缫�ĵ缫��ӦΪ��O2+2H2O+4e-�T4OH- | |
| C�� | ȼ�ϵ���е������Һ��pH���ֲ��� | |
| D�� | d�缫������ų� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ĵ��ʼ��仯�����ڹ�ũҵ����������������Ҫ�����ã�
������ĵ��ʼ��仯�����ڹ�ũҵ����������������Ҫ�����ã��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com