
分析 (1)①依据m=CVM计算需要溶质的质量;
②依据配制一定物质的量浓度溶液的一般步骤(计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶、贴标签)选择需仪器:
③依据配制一定物质的量浓度溶液的一般步骤解答;
(2)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(3)不当操作导致实验失败的,且无法补救的需要重新配制;
(4)该反应中,锰元素的化合价由+7价变为+2价,铁元素的化合价由+2价变为+3价,依据氧化还原反应化合价升级数目相等,原子个数守恒配平方程式;
依据方程式:1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O,可知MnO4-~5Fe2+,据此计算硫酸亚铁的物质的量浓度.
解答 解:(1)①配制100mL 0.5mol/L的KMnO4溶液,需要高锰酸钾的质量m=0.5mol/L×0.1L×158g/mol=7.9g;
②配制100mL 0.5mol/L的KMnO4溶液的一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶、贴标签,用到的仪器:托盘天平、药匙、烧杯、玻璃杯、100mL容量瓶、胶头滴管;
所以还缺少的仪器:玻璃杯、100mL容量瓶、胶头滴管;
故答案为:玻璃杯、100mL容量瓶、胶头滴管;
③配制100mL 0.5mol/L的KMnO4溶液的一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀;
故答案为:溶解、定容;
(2)①称量时使用了游码,而试剂与砝码的左右位置颠倒,实际称得固体质量为砝码减去游码的质量,质量偏小,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
②定容时,仰视刻度线,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏低;
③配制过程中未洗涤烧杯和玻璃棒,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
(3)配制0.5mol/L的KMnO4溶液,定容时不慎加水超过了刻度线,实验失败且无法补救,必须重新配制;
故答案为:重新配制;
(4)该反应中,锰元素的化合价由+7价变为+2价,铁元素的化合价由+2价变为+3价,要使氧化剂得到电子数等于还原剂失去电子数则:高锰酸根离子系数为1,二价铁离子系数为5,依据原子个数守恒方程式:1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O;
10mL 0.5mol/L的KMnO4溶液含义高锰酸钾物质的量为:0.5mol/L×0.01L=0.005mol,依据MnO4-~5Fe2+,消耗二价铁离子物质的量为:0.005mol×5=0.025mol,则硫酸亚铁的物质的量为0.025mol,物质的量浓度为:$\frac{0.025mol}{0.02L}$=1.25mol/L;
故答案为:1,5,8,1,5,4;1.25mol/L.
点评 本题为综合题,考查了一定物质的量浓度溶液配制、氧化还原方程式配平及氧化还原滴定,明确配制原理及操作步骤,熟悉氧化还原反应滴定中反应物之间关系是解题关键,题目难度中等.


科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 氧化性Cl2>Br2>I2还原性Cl->Br->I- | |
| C. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| D. | 氯水具有酸性,能使紫色石蕊试剂先变红后褪色,也可用pH试纸测量其pH值 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
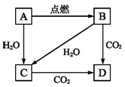 如图所示A是固体金属单质,燃烧时火焰呈黄色.
如图所示A是固体金属单质,燃烧时火焰呈黄色.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室用氢氧化钠固体配制1.0mol•L-1的NaOH溶液250mL,回答下列问题:
实验室用氢氧化钠固体配制1.0mol•L-1的NaOH溶液250mL,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解可以得到氯乙烯 | |
| B. | 油脂水解可得到氨基酸和甘油 | |
| C. | 所有烷烃和蛋白质中都存在碳碳单键 | |
| D. | 淀粉和纤维素水解的最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 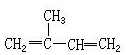 2-甲基-1,3-丁二烯 2-甲基-1,3-丁二烯 | B. | 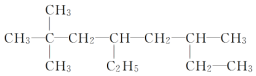 2,2-二甲基-4,6-二乙基庚烷 2,2-二甲基-4,6-二乙基庚烷 | ||
| C. |  1,3,4-三甲苯 1,3,4-三甲苯 | D. |  2-甲基-3-戊烯 2-甲基-3-戊烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com