
【题目】Mg和Mg2+两种微粒中,具有相同的
A.核内质子数B.核外电子数C.最外层电子数D.核外电子层数
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期数与其主族序数相等。

回答下列问题:
(1)T的原子结构示意图为____。
(2)R元素的名称为____
(3)元素W在周期表中的位置:____________
(4)W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成两种物质,其中一种是气体,发生反应的化学方程式为__________。
(5)原子序数比R大1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答:
(1)H2O2的电子式 .
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由 .
(3)完成以下氧化还原反应的离子方程式:MnO﹣4+C2O2﹣4+=Mn2++CO2↑+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析: 
(1)该反应的化学方程式为;
(2)反应从开始至2分钟末,用Z表示该反应的平均反应速率;
(3)反应达平衡时X的转化率: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种名样,如图是扇形元素周期表的一部分,下列说法正确的是

A. 简单氢化物的沸点: ④>⑤>⑨
B. 该表中标注的元素⑩处于第四周期ⅦB族
C. 元素⑥和⑦的原子序数相差11
D. 同温同压下,等质量的由元素⑤形成的两种气体单质含有相同的原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍.湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品.某化学小组模拟该方法回收铜和制取胆矾,流程简图如下: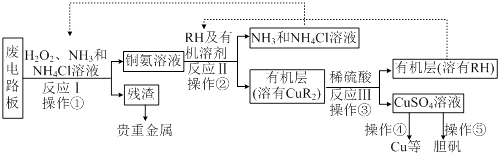
回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)2+4,反应中H2O2 的作用是 .
(2)反应II是铜氨溶液中的Cu(NH3)2+4与有机物RH反应,写出该反应的离子方程式: . 操作②用到的主要仪器名称为 , 其目的是(填序号) .
a.富集铜元素 b.使铜元素与水溶液中的物质分离 c.增加Cu2+在水中的溶解度
(3)操作④以石墨作电极电解CuSO4 溶液.阴极析出铜,阳极产物是 . 操作⑤由硫酸铜溶液制胆矾的主要步骤是 .
(4)流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下: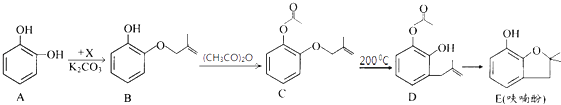
(1)A物质核磁共振氢谱共有个峰,B→C的反应类型是 .
(2)已知x的分子式为C4H7C1,写出A→B的化学方程式: .
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y的名称(系统命名)是 .
(4)下列有关化合物C、D的说法正确的是 . ①可用氯化铁溶液鉴别C和D
②C和D含有的官能团完全相同
③C和D互为同分异构体
④C和D均能使溴水褪色
(5)E的同分异构体很多,写出一种符合下列条件的芳香族同分异构体的结构简式: . ①环上的一氯代物只有一种 ②含有酯基 ③能发生银镜反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据高中所学的化学反应原理解答下面的问题:
(1)下面为CO2加氢制取低碳醇的热力学数据:
反应Ⅰ:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0 kJmol﹣1
反应Ⅱ:2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g)△H=﹣173.6kJmol﹣1
写出由CH3OH(g)合成CH3CH2OH(g)的热化学反应方程式:
(2)工业合成甲醇的反应:CO(g)+2H2(g)CH3OH(g)△H<0.
①该反应在不同温度下的化学平衡常数(K)如下表:
温度/℃ | 250 | 350 |
K | 2.041 | x |
符合表中的平衡常数x的数值是(填字母序号).
A.0 B.0.012
C.32.081 D.100
②若装置乙为容积固定的密闭容器,不同时间段各物质的浓度如下表:
c(CO) | c(H2) | c(CH3OH) | |
0min | 0.8molL﹣1 | 1.6molL﹣1 | 0 |
2min | 0.6molL﹣1 | y | 0.2molL﹣1 |
4min | 0.3molL﹣1 | 0.6molL﹣1 | 0.5molL﹣1 |
6min | 0.3molL﹣1 | 0.6molL﹣1 | 0.5molL﹣1 |
反应从2min到4min之间,H2的平均反应速率为 . 反应达到平衡时CO的转化率为 . 反应在第2min时改变了反应条件,改变的条件可能是(填字母序号).
A.使用催化剂 B.降低温度 C.增加H2的浓度 D.升高温度
(3)全钒液流储能电池(VRB)广泛应用于风能、太阳能发电系统的储能系统,电池反应为VO2++V2++2H+ ![]() VO2++V3++H2O,试推写出放电时正极的电极反应式 .
VO2++V3++H2O,试推写出放电时正极的电极反应式 .
(4)如图2为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况.据图分析:该温度下,溶度积常数的关系为:Ksp[Fe(OH)3] Ksp[Mg(OH)2](填:>、=、<);如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+ , 振荡后,白色沉淀会全部转化为红褐色沉淀,原因是 . 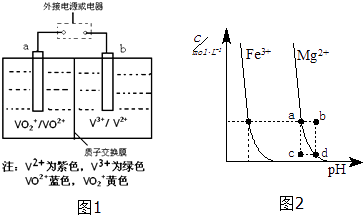
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com